
| A. | H+、Na+、HCO3-、Cl- | B. | Fe3+、SCN-、Cl-、NO3- | ||
| C. | Mg2+、Cu2+、SO42-、NO3- | D. | Fe2+、SO42-、H+、NO3- |
分析 A.氢离子与碳酸氢根离子反应;
B.铁离子与硫氰根离子反应生成络合物硫氰化铁;
C.四种离子之间不反应,能够共存;
D.硝酸根离子在酸性条件下能够氧化亚铁离子.
解答 解:A.H+、HCO3-之间反应生成二氧化碳气体和水,在溶液中不能大量共存,故A错误;
B.Fe3+、SCN-之间反应生成硫氰化铁,在溶液中不能大量共存,故B错误;
C.Mg2+、Cu2+、SO42-、NO3-之间不反应,在溶液中能够大量共存,故C正确;
D.Fe2+、H+、NO3-之间发生氧化还原反应,在溶液中不能大量共存,故D错误;
故选C.
点评 本题考查离子共存的判断,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况,ru:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.


 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案科目:高中化学 来源: 题型:解答题
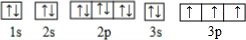 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 以极性键结合起来的分子一定是极性分子 | |
| B. | 非极性分子中,一定含有非极性共价键 | |
| C. | 乙醇分子和水分子间只存在范德华力 | |
| D. | 卤素单质按F2→I2,熔沸点逐渐升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ③ | C. | ①② | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶解度(s) | B. | 物质的量浓度(c) | C. | 质量分数(w) | D. | 摩尔质量(M) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

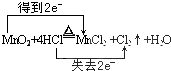 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
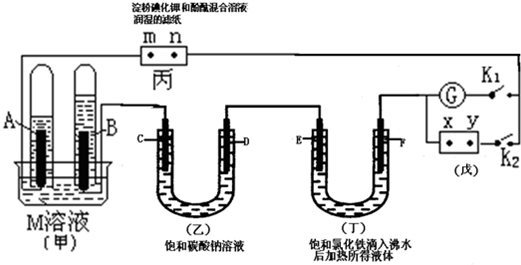
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol Na2SiO3中含有NA个Na2O | |
| B. | 在H2O2+Cl2═2HCl+O2反应中,每生成32 g氧气,则转移NA个电子 | |
| C. | 标准状况下,分子数为NA的CO、C2H4混合气体体积约22.4 L,质量为28 g | |
| D. | 4.6 g Na与适量氧气完全反应生成Na2O、Na2O2,反应中转移的电子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com