
【题目】氮的氧化物既是空气的重要污染物,同时也是重要的化工原料。
(1)在373K时,向体积为2L的恒容真空容器中通入0.40molNO2,发生反应:2NO2(g)![]() N2O4(g) ΔH=57.0kJ·mol1。测得NO2的物质的量分数[φ(NO2)]与反应时间(t)的关系如下表:
N2O4(g) ΔH=57.0kJ·mol1。测得NO2的物质的量分数[φ(NO2)]与反应时间(t)的关系如下表:
t/min | 0 | 20 | 40 | 60 | 80 |
φ(NO2) | 1.0 | 0.75 | 0.52 | 0.40 | 0.40 |
①0~20 min内,υ(N2O4)=___mol·L1·min1。
②上述反应中,υ正(NO2)=k1·c2(NO2),υ逆(N2O4)=k2·c(N2O4),其中k1、k2为速率常数,则373K时,k1、k2的数学关系式为___。改变温度至T1时k1=k2,则T1__373K(填“>”“<”或“=”)。
(2)NH3催化还原氮氧化物是目前应用广泛的烟气脱硝技术。已知:6NO2(g)+8NH3(g)![]() 7N2(g)+12H2O(l) ΔH,向容积为2L的恒容密闭容器中,充入NO2和NH3的混合气体0.14mol充分反应。不同投料比时,NO2的平衡转化率与温度的关系如图中曲线所示[投料比=n(NO2)/n(NH3)]。
7N2(g)+12H2O(l) ΔH,向容积为2L的恒容密闭容器中,充入NO2和NH3的混合气体0.14mol充分反应。不同投料比时,NO2的平衡转化率与温度的关系如图中曲线所示[投料比=n(NO2)/n(NH3)]。
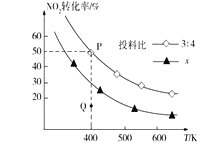
①ΔH___0(填“>”“<”或“=”)。
②x___3∶4(填“>”“<”或“=”)。
③400K时,反应的平衡常数为___(填计算式即可)。
④投料比为3∶4时,Q点υ逆(NH3)___(填“>”“<”或“=”)P点υ逆(NH3)。
【答案】2.0×103 k1=60k2 > < > ![]() <
<
【解析】
(1)①根据表中数据计算NO2的消耗速率,再由化学计量比计算N2O4的生成速率;
②反应达到平衡时有υ正=υ逆,据此计算,反应为放热反应,温度升高,不利于反应正向进行;
(2)①投料比一定时,升高温度二氧化氮转化率减小,平衡逆向移动,则正反应放热;
②温度相同时,增大投料比,二氧化氮转化率减小;
③根据图像,400 K时,投料比3:4时,达到平衡NO2的转化率为50%,列出三段式,结合K的表达式计算;
④投料比为3:4时,温度相同,Q点没有达到平衡状态,要使反应达到平衡状态二氧化氮转化率应该增大,平衡正向移动,P点为平衡状态;
(1)①反应为:2NO2(g)![]() N2O4(g),
N2O4(g),
起始(mol) 0.40 0
转化(mol) 2x x
20min(mol) 0.40-2x x
20min时,NO2的体积分数为0.75,所以 ![]() =0.75,可得x=0.08,所以反应20min时,消耗NO2的物质的量为0.08×2mol=0.16mol,0~20min内,NO2的消耗速率为υ(NO2)=
=0.75,可得x=0.08,所以反应20min时,消耗NO2的物质的量为0.08×2mol=0.16mol,0~20min内,NO2的消耗速率为υ(NO2)=![]() =4×10-3mol/(L·min), 根据化学计量比等于反应速率之比,则υ(N2O4)=
=4×10-3mol/(L·min), 根据化学计量比等于反应速率之比,则υ(N2O4)= ![]() υ(NO2)=2×10-3mol/(L·min);
υ(NO2)=2×10-3mol/(L·min);
②反应达到平衡时有υ正=υ逆,即υ正(NO2)=2υ逆(N2O4),达到平衡时,NO2的体积分数为0.40,即( 0.4-2x )÷(0.4-x) =0.4,可得x=0.15,所以化学平衡常数为K= c(N2O4)÷c2(NO2) =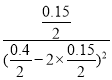 =30,则有k1·c2(NO2)=2k2·c(N2O4),所以k1= 2k2c(N2O4) ÷c2(NO2) =60k2, 改变温度至T1时k1=k2,由于k1=2k2·K,则K=
=30,则有k1·c2(NO2)=2k2·c(N2O4),所以k1= 2k2c(N2O4) ÷c2(NO2) =60k2, 改变温度至T1时k1=k2,由于k1=2k2·K,则K=![]() ,平衡常数减小,正反应为放热反应,温度升高,不利于反应正向进行,所以温度应为升高,即T1>373K;
,平衡常数减小,正反应为放热反应,温度升高,不利于反应正向进行,所以温度应为升高,即T1>373K;
(2)①投料比一定时,升高温度二氧化氮转化率减小,平衡逆向移动,则正反应放热,所以△H<0;
②温度相同时,增大投料比,二氧化氮转化率减小,温度相同时二氧化氮转化率x较小,说明投料比x>3:4;
③根据图像,400 K时,投料比3:4时,达到平衡NO2的转化率为50%,列三段式
6NO2(g)+8NH3(g)![]() 7N2(g)+12H2O(l)
7N2(g)+12H2O(l)
c(起始)(mol/L)0.03 0.04 0
c(转化)(mol/L)0.03×0.5 0.02 0.0175
c(平衡)(mol/L)0.015 0.02 0.0175
反应的平衡常数K=![]() ;
;
④投料比为3:4时,温度相同,Q点没有达到平衡状态,要使反应达到平衡状态二氧化氮转化率应该增大,平衡正向移动,P点为平衡状态,所Q点υ逆(NH3)<P点υ逆(NH3)。


 一线名师提优试卷系列答案
一线名师提优试卷系列答案科目:高中化学 来源: 题型:
【题目】A~H分别表示中学化学中常见的某种物质,它们之间的相互转化关系如下图所示(部分反应物、生成物未列出)。已知:C、D、E、F、G五种物质中均含有同一种元素;A为淡黄色固体化合物;G为红褐色固体。

(1)写出化学式:A:________________;C:________________;F:________________。
(2)写出反应的化学方程式:
②_____________________________________________________________。
⑥_____________________________________________________________。
(3)写出离子方程式:
③_____________________________________________________________。
⑤_____________________________________________________________。
(4)生成24 g B需要转移________mol电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用海水可以提取溴和镁,提取过程如下。
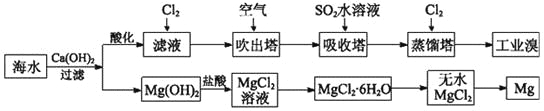
(1)提取溴的过程中,经过两次Br-→Br2转化的目的是________,吸收塔中发生反应的离子方程式是__________。用平衡移动原理解释通空气的主要目的是_______。
(2)从MgCl2溶液中得到MgCl2·6H2O晶体的主要操作是________________、过滤、洗涤、干燥。
(3)依据上述流程,若将10 m3海水中的溴元素转化为工业溴,至少需要标准状况下Cl2的体积为________L(忽略Cl2的溶解)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】18.4 g 氢氧化钠和碳酸氢钠固体混合物,在密闭容器中加热到250 ℃,经充分反应后排出气体,冷却,称得剩余固体质量为16.6 g。试计算原混合物中碳酸氢钠的质量分数。________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在石蜡油的分解实验中,产物可使酸性高锰酸钾溶液褪色,也可以使溴的四氯化碳溶液褪色。
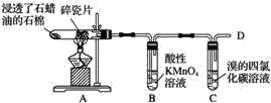
请你根据实验过程及现象探讨下列问题:
(1)碎瓷片的作用是__。
(2)分解产物中的气体是否都是烷烃__,你的依据是__。
(3)证明石蜡油分解产物中含有碳、氢元素的方法是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤炭是重要的化工原料,但属于不可再生能源,高效、清洁地利用煤炭资源至关重要。请回答下列问题:
(1)煤的气化。原理是C(s)+2H2(g)![]() CH4(g) ΔH。
CH4(g) ΔH。
在1L密闭容器中投入1mol碳,并充入2molH2,测得相关数据如图所示。
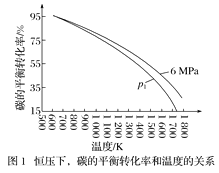

①有关图1、图2的说法正确的有___(填字母)。
a.p1<6MPa b.T1<1000K
c.ΔH<0 d.工业生产中,当温度为T2时,压强越高,经济效益越好
②图2中A点对应的平衡常数Kp=__(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(2)煤生产水煤气和半水煤气。
①工业上用煤生产作为合成氨原料气的水煤气,要求气体中(CO+H2)与N2的体积之比为3.1~3.2,发生的反应有C(s)+H2O(g)![]() CO(g)+H2(g),C(s)+
CO(g)+H2(g),C(s)+![]() O2(g)
O2(g)![]() CO(g)。从能量角度考虑,通入空气的目的是___。
CO(g)。从能量角度考虑,通入空气的目的是___。
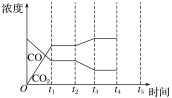
②如图是反应CO(g)+H2O(g)![]() H2(g)+CO2(g) ΔH<0中CO和CO2的浓度随时间发生变化的曲线,则t2时刻改变的条件可能是___(写出1种即可)。若t4时刻通过改变容积的方法将压强增大为原来的2倍,在图中t4~t5区间内画出CO、CO2浓度变化曲线,并标明物质名称(假设各物质状态均保持不变)。___
H2(g)+CO2(g) ΔH<0中CO和CO2的浓度随时间发生变化的曲线,则t2时刻改变的条件可能是___(写出1种即可)。若t4时刻通过改变容积的方法将压强增大为原来的2倍,在图中t4~t5区间内画出CO、CO2浓度变化曲线,并标明物质名称(假设各物质状态均保持不变)。___
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I-可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程如下。i.SO2+4I-+4H+![]() S↓+2I2+2H2O ii.I2+2H2O+SO2
S↓+2I2+2H2O ii.I2+2H2O+SO2![]() SO42- +4H++2I-
SO42- +4H++2I-
探究i、ii反应速率与SO2歧化反应速率的关系,实验如下:分别将18 mL SO2饱和溶液加入到2 mL下列试剂中,密闭放置观察现象。(已知:I2易溶解在KI溶液中)
序号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
试剂组成 | 0.4 mol·L-1 KI | a mol·L-1 KI 0.2 mol·L-1 H2SO4 | 0.2 mol·L-1 H2SO4 | 0.2 mol·L-1 KI 0.0002 mol I2 |
实验现象 | 溶液变黄,一段时间后出现浑浊 | 溶液变黄,出现浑浊较A快 | 无明显现象 | 溶液由棕褐色很快褪色,变成黄色,出现浑浊较A快 |
下列说法不正确的是( )
A. 水溶液中SO2歧化反应方程式为3SO2+2H2O ![]() 2H2SO4 +S↓
2H2SO4 +S↓
B. II是I的对比实验,则a=0.4
C. 比较I、II、III,可得出的结论是:I是SO2歧化反应的催化剂,H+单独存在时不具有催化作用,但H+可以加快歧化反应速率
D. 实验表明,SO2的歧化反应速率IV>I,原因是反应i比ii快;IV中由反应ii产生的H+使反应i加快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是氢氧燃料电池的示意图,按图中提示,下列叙述不正确的是( )

A. a电极是负极,b电极是正极
B. a电极的电极反应式为H2-2e-===2H+
C. b电极的电极反应式为4OH--4e-===2H2O+O2↑
D. 氢氧燃料电池不需要将还原剂和氧化剂全部储藏在电池内
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】地奥司明片是治疗静脉淋巴功能不全相关的各种症状(腿部沉重、疼痛、晨起酸胀不适感)的主要治疗药物,下图为合成地奥司明片重要中间体,下列有关说法正确的是( )

A. 分子式为C18H20O6
B. 该中间体是高分子化合物
C. 该中间体可发生水解反应生成乙醇
D. 该中间体分子在一定条件下可以发生取代、加成、氧化反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com