
| A. | 黄砷的熔点高于白磷 | B. | 黄砷中共价键键能大于白磷 | ||
| C. | 黄砷分子极性大于白磷 | D. | 分子中共价键键角均为109°28′ |
科目:高中化学 来源: 题型:选择题
| A. | 垃圾分类并回收利用,符合可持续发展的要求,是垃圾处理的发展方向 | |
| B. | 人类活动排入大气的氟氯代烷和含溴的卤代烃能使臭氧层受到破坏 | |
| C. | 防止水体污染和改善水质最根本的措施是控制工业废水和生活污水的排放 | |
| D. | 目前常用的垃圾处理方法有卫生填埋、堆肥和焚烧,这些方法对环境无污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在保持体积不变的条件下,充入较多的乙苯,可以提高乙苯的转化率 | |
| B. | 在保持压强不变的条件下,充入不参加反应的气体,可以提高乙苯的转化率 | |
| C. | 在反应达到平衡过程中,体系的平均相对分子质量在不断增大 | |
| D. | 仅从平衡移动的角度分析,工业生产苯乙烯选择恒容条件优于恒压条件 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2LCO和2LCO2 | B. | 标准状况下22.4LH2O和1mol O2 | ||
| C. | 0,4克H2和4.48L HCl | D. | 18克水和标准状况下22.4L CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
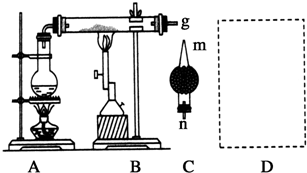
 某学习小组探究溴乙烷的消去反应并验证产物.
某学习小组探究溴乙烷的消去反应并验证产物.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com