
����Ŀ������ʯ��������������(Na3A1F6)��ɫ���壬����ˮ���������������ҵ�����ۼ�����ҵ����өʯ(��Ҫ�ɷ���CaF2)��Ũ���ᡢ����������̼������Һͨ��ʪ���Ʊ�����ʯ��ij��ѧʵ��С��ģ�ҵ����ȡNa2AlF6��װ��ͼ����(��װ�þ��ɾ��ķ���ϩ������װ����)��
��֪��CaF2+H2SO4![]() CaSO4+2HF��
CaSO4+2HF��
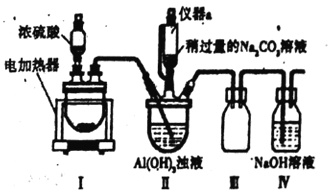
(1)ʵ����������ʹ�ò���������ԭ����_____________(�û�ѧ����ʽ��ʾ)��
(2)װ��III������Ϊ______________________��
(3)��ʵ������У�װ��II����CO2�����ݳ���ͬʱ�۲쵽�а�ɫ������������д���÷�Ӧ�����ӷ�Ӧ����ʽ��__________________��
(4)��ʵ������У�����װ��II��ͨ��HF���壬Ȼ���ٵμ�Na2CO3��Һ���������Ƚ�Na2CO3��A1(OH)3��Ϻ���ͨ��HF���壬��ԭ����_______________�� .
(5)װ��II��Ӧ��Ļ��Һ�������˿ɵõ�Na3A1F6���壬�ڹ��˲�����ȷ�������Ѿ�ϴ�Ӹɾ��ķ�����_____________________��
(6)�ڵ�������Ĺ�ҵ�����У������ĵ缫��ӦʽΪ_____________��
(7)өʯ�к���������Fe2O3���ʣ�������װ��I��Ӧ�����Һ���ⶨ�����Ƶĺ���������������£�ȡ8.0 gөʯ����װ��I�У���ȫ��Ӧ�����Һ��ϡ�ͣ�Ȼ�����������KI���壬���Ե���Ϊָʾ������0.1000 mol��L-1 Na2S2O3����Һ�ζ���������_________����ʱ������ζ��յ㣬����Na2S2O3����Һ40.00mL����өʯ�з����Ƶİٷֺ���Ϊ______________��(��֪:I2+2S2O32-==S4O62-+2I-)
���𰸡� 4HF + SiO2==SiF4+2H2O ��Ϊ��ȫƿ����ֹ���� 2Al(OH)2 + 12HF+6Na++3CO32-==2Na3AlF4��+3CO2��+9H2O ̼������Һ�ʼ��ԣ�Na2CO3��������HF��Ӧ��������Al(OH)3���ܽ� ȡ���һ��ϴ��Һ�������Թ��У������еμ�BaCl2��Һ�����ް�ɫ�������ɣ�˵��������ϴ�Ӹɾ� 2O2--4e-==O2�� ��Һ��ɫ��ȥ���Ұ�����ڲ��ָ� 96%
�����������������������Ҫ���������ȡNa2AlF6ʵ������ۡ�
(1)������벣���ɷֶ������跴Ӧ����ʴ������4HF + SiO2==SiF4+2H2O��
(2)װ��III�������Ƿ�ֹ������
(3)�ð�ɫ����������ˮ�����������ƣ��÷�Ӧ�����ӷ�Ӧ����ʽ��2Al(OH)2 + 12HF+6Na++3CO32-==2Na3AlF4��+3CO2��+9H2O��
(4)��ԭ����Na2CO3��������HF��Ӧ��������Al(OH)3���ܽ⡣
(5)��������Na+��CO32-�����ӣ����Լ���CO32-���ڹ��˲�����ȷ�������Ѿ�ϴ�Ӹɾ��ķ�����ȡ���һ��ϴ��Һ�������Թ��У������еμ�BaCl2��Һ�����ް�ɫ�������ɣ�˵��������ϴ�Ӹɾ���
(6)�ڵ�������Ĺ�ҵ�����У������ĵ缫��ӦʽΪ2O2--4e-==O2����
(7) Fe2O3�ܽ������Fe3+��KI����ΪI2��I2�����۱�������������Һ��ɫ��ȥ���Ұ�����ڲ��ָ�����ʱ������ζ��յ㡣Fe2O3��2Fe3+��I2��2S2O32-��n(Fe2O3)= 0.5n(Na2S2O3)=0.50.1000 mol/L��0.040L=0.0040mol��m(Fe2O3)= 0.0020mol��160g/mol=0.32g����өʯ�з����Ƶİٷֺ���Ϊ1-0.32/8.0=96%��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��SiH4��һ����ɫ���壬���������ܷ�����ը����ȼ������SiO2��Һ̬ˮ����֪������2g SiH4��ȼ�ų�����89.2kJ��SiH4��ȼ���Ȼ�ѧ����ʽΪ______________________________��
��2��д���ö��Ե缫��ⱥ��ʳ��ˮ���ܵ�����ӷ���ʽ��_________________��
��3��д���ö��Ե缫�������ͭ��Һ���ܻ�ѧ����ʽ��___________ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ����̼��һ����;�൱�㷺�Ļ�������ԭ�ϡ����Ի�ԭ������������������ϳɺܶ��л�����״���CH3OH���������ѣ�CH3OCH3���ȣ���������ȼ�ϡ�
(1)��ѹǿΪ0.1 MPa�����£���a mol CO��3a mol H2�Ļ�������ڴ������������Է���Ӧ���ɼ״��� CO(g)��2H2(g) ![]() CH3OH(g) ��H<0
CH3OH(g) ��H<0
�� �÷�Ӧ��ƽ�ⳣ������ʽΪ____________��
�� �������ݻ����䣬���д�ʩ�����Ӽ״����ʵ���___________��
A�������¶� B����CH3OH(g)����ϵ�з���
C������He��ʹ��ϵ��ѹǿ���� D���ٳ���1 mol CO��3 mol H2
(2����֪���� CO(g)��2H2(g) ![]() CH3OH(g) ��H1 ����90.7 kJ��mol��1
CH3OH(g) ��H1 ����90.7 kJ��mol��1
�� 2CH3OH(g) ![]() CH3OCH3(g)��H2O(g) ��H2 ����23.5 kJ��mol��1
CH3OCH3(g)��H2O(g) ��H2 ����23.5 kJ��mol��1
�� CO(g)��H2O(g) ![]() CO2(g)��H2(g) ��H3 ����41.2 kJ��mol��1
CO2(g)��H2(g) ��H3 ����41.2 kJ��mol��1
�� 3CO(g)��3H2(g) ![]() CH3OCH3(g)��CO2(g)�� ��H ��_______kJ��mol��1
CH3OCH3(g)��CO2(g)�� ��H ��_______kJ��mol��1
(3)�״�Ҳ������Դ��ص�ȼ�ϣ�������ˮ�ʻ����һ������Ⱦ����һ�ֵ绯ѧ��������������Ⱦ����ԭ���ǣ� 2�μ״���1mL 1.0mol��L��1���ᣬ4mL 0.1mol��L��1������ (CoSO4�������Һ�������������Ե缫��ͨ�磬��Co2+������Co3+��Ȼ����Co3+����������ˮ�еļ״�������CO2��������ʵ������ͼװ��ģ���������̣�
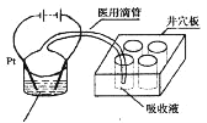
�� ������ʱ������CO2���壬��Ѩ��Ѩ����Ӧʢ��___________��Һ��
�� д�������״������ӷ���ʽ______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ļ�ѧʽΪ(CN)2���ṹʽΪN��C-C��N��������±�����ƣ�����������ȷ���ǣ� ��
A.��������������Һ������Ӧ
B.������N��C���ļ�������C��C���ļ���
C.�����м��м��Լ������зǼ��Լ�
D.�������2��������4������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E��ԭ������������������ֳ���Ԫ�أ�����A��ԭ�Ӱ뾶��С��Ԫ�أ�BԪ�ص�һ�ֺ��ؿ����ڿ��Ŷϴ���DԪ�ص�s�����p����ϵĵ������������2��δ�ɶԵ��ӣ�E�ǵ�������Ԫ�أ���ԭ�Ӻ���������������Aԭ����ͬ�����������Ӿ�����������Ԫ�ط��Ż�ѧʽ�ش��������⣺
��1��A��B��C��D����Ԫ���У��縺��������___����һ������������___��
��2��������CA3�ķе�Ȼ�����BA4�ĸߣ�����Ҫԭ����____��
��3��A��B�γɵĻ�����M��������(HCN)��Ӧ�ɵñ�ϩ��(H2C=CH��C��N)����M�ĽṹʽΪ___����ϩ�������̼ԭ�ӹ���ӻ�������____��
��4����CԪ���γɵ�һ��������BD2��Ϊ�ȵ����壬�����ӵĽṹʽΪ____��
��5����̬Eԭ�ӵĺ�������Ų�ʽΪ____����ͼ��D��E�γɵ�ij�ֻ�����ľ����ṹʾ��ͼ���þ���Ļ�ѧʽΪ____��
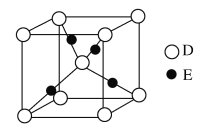
��6����E����������Һ��ͨ�������CA3��������[E(CA3)4]2����1mol[E(CA3)4]2���к�����������ĿԼΪ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ϳ�NH3�����H2����ú��H2O��Ӧ�Ƶã�������һ����ӦΪ��CO��g��+H2O��g��![]() CO2��g��+H2��g�� ��H��O�������COת���ʿɲ��õķ��������Тٽ����¶Ȣ�����ѹǿ��ʹ�ô���������CO��Ũ�Ȣ�����ˮ������Ũ�ȣ�������ȷ������ǣ� ��
CO2��g��+H2��g�� ��H��O�������COת���ʿɲ��õķ��������Тٽ����¶Ȣ�����ѹǿ��ʹ�ô���������CO��Ũ�Ȣ�����ˮ������Ũ�ȣ�������ȷ������ǣ� ��
A. �٢ڢ�B. �ܢ�C. �٢�D. ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܱ�������һ�����Ļ�����巢����ӦxA(g)+yB(g)![]() zC(g)��ƽ��ʱ���A��Ũ��Ϊ0.50 mol/L�������¶Ȳ���.���������ݻ�����ԭ�����������ٴ�ƽ��ʱ�����A��Ũ�Ƚ���Ϊ0.30 mol/L�������й��ж���ȷ����
zC(g)��ƽ��ʱ���A��Ũ��Ϊ0.50 mol/L�������¶Ȳ���.���������ݻ�����ԭ�����������ٴ�ƽ��ʱ�����A��Ũ�Ƚ���Ϊ0.30 mol/L�������й��ж���ȷ����
A.B��ת���ʽ���B.ƽ��������Ӧ�����ƶ�
C.x+y<zD.C�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
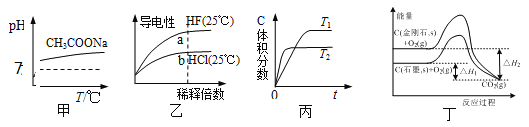
A. ��ͼ��֪�������¶ȴ����Ƶ�ˮ��̶�����
B. ��ͼ�ҿ�֪��a��Kw����ֵ��b��Kw����ֵ��
C. ��ͼ����֪����ӦA(g)+B(g) ![]() 2C(g)�����ȷ�Ӧ
2C(g)�����ȷ�Ӧ
D. ��ͼ����֪����ӦC(���ʯ��s)= C(ʯī��s)���ʱ���H=��H1����H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��ӦCO(g)+H2O(g)![]() CO2(g)+H2(g) ��H<0����һ���¶Ⱥ�ѹǿ�����ܱ������У���Ӧ�ﵽƽ�⡣����������ȷ���ǣ� ��
CO2(g)+H2(g) ��H<0����һ���¶Ⱥ�ѹǿ�����ܱ������У���Ӧ�ﵽƽ�⡣����������ȷ���ǣ� ��
A.�����¶ȣ�n(CO)����B.��Сѹǿ��n(CO2)����
C.������Ч������CO��ת��������D.����һ�����ĵ�����n(H2)����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com