
| A. | Fe | B. | Mg | C. | Al | D. | Zn |
分析 稀硫酸浓度降低,说明金属与稀硫酸反应生成氢气,令金属的相对原子质量为a、反应中化合价为b,消耗一般硫酸时金属有剩余,根据电子转移守恒列不等式,结合选项讨论确定.
解答 解:参加反应的硫酸物质的量=0.1L×2mol/L×$\frac{1}{2}$=0.1mol,设金属的相对原子质量为a、反应中化合价为b,金属还没有全部溶解,根据电子转移守,则$\frac{5}{a}$×b>0.1×2,
A.反应中Fe为+2价,则a<$\frac{5×2}{0.2}$=50,故A不符合;
B.反应中Mg为+2价,则a<$\frac{5×2}{0.2}$=50,故B符合;
C.应中Al为+3价,则a<$\frac{5×3}{0.2}$=75,故C符合;
D.反应中Zn为+2价,则a<$\frac{5×2}{0.2}$=50,故D不符合;
故选BC.
点评 本题考查根据方程式计算、氧化还原反应计算,难度不大,注意利用电子转移守恒方法简化计算,注意讨论法的利用,试题培养了学生的化学计算能力.


 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | CH3CH2CH2Cl | B. | CH3CHBrCH2Br | C. | CH2BrCH2CH2Br | D. | CH3CHBrCH2CH2Br |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①③ | C. | ②③ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳素钢、不锈钢、硬铝、黄铜都属于合金 | |
| B. | 正常雨水的pH为5.6,主要是因为溶解了SO2 | |
| C. | 钢化玻璃常用于制造眼镜片、照相机中的透镜等 | |
| D. | 光化学烟雾主要是由于向大气中任意排放CO2、氟氯烃、SO2等产生的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
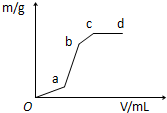 向用盐酸酸化的MgSO4溶液中加入Ba(OH)2溶液,产生的沉淀质量m与加入的体积V之间的关系,关于图曲线的推测正确的是( )
向用盐酸酸化的MgSO4溶液中加入Ba(OH)2溶液,产生的沉淀质量m与加入的体积V之间的关系,关于图曲线的推测正确的是( )| A. | ab段产生的沉淀为硫酸钡 | |
| B. | ab产生段的沉淀为氢氧化镁 | |
| C. | bc段产生的沉淀为氢氧化镁 | |
| D. | bc段产生的沉淀为硫酸钡和氢氧化镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu与Cu20的物质的量之比为2:1 | |
| B. | 硝酸的物质的量浓度为2.4mol/L | |
| C. | 产生的NO在标准状况下的体枳为4.48L | |
| D. | Cu、Cu20与硝酸反应后剩余HN03为lmol |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 4FeS2( s)+11O2( g)═2Fe2O3( s)+8SO2(g)△H=-3414.8kJ•moL | |
| B. | FeS2(s)+$\frac{11}{4}$O2(g)═$\frac{1}{2}$Fe2O3 (s)+2SO2(g)△H=-853.7kJ•moL | |
| C. | 4FeS2(s)+11O2(g)═2 Fe2O3 (s)+8SO2(g)△H+3414.8kJ•moL | |
| D. | FeS2(s)+$\frac{11}{4}$O2(g)═$\frac{1}{2}$Fe2O3 (s)+2SO2(g)△H=+853.7kJ•moL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com