
(9分)X~R是元素周期表中的短周期元素,其相关信息如下表:
元素 | X | Y | Z | W | R |
相关信息 | 能形成+7价的化合物 | 日常生活中常见的金属,熔化时并不滴落,好像有一层膜兜着 | 通常状况下能形成短周期中最稳定的双原子分子 | 焰色反应为黄色 | 最外层有二个未成对电子,无正价 |
请用化学用语回答下列问题:
(1)基态原子X的核外电子所处最高能层的能层符号是 。
(2)Z的氢化物的电子式 ,中心原子的杂化类型是 ,元素Z、R的气体氢化物的稳定性顺序是 ,Z的氢化物易液化,原因是 。
(3)R的某种氢化物C有18个电子,工业上利用电解KHSO4水溶液所得的产物与水反应制备C。电解KHSO4水溶液时(该条件下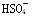 部分电离),阳极反应式是
部分电离),阳极反应式是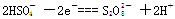 ,阴极反应式是 ;已知1mol
,阴极反应式是 ;已知1mol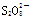 与水反应得到C时转移了2 mol e-,则该反应的离子方程式是 。
与水反应得到C时转移了2 mol e-,则该反应的离子方程式是 。
(1) M (2) 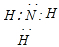 ,SP3 NH3﹤H2O,NH3 分子间有氢键,增加了分子间作用力
,SP3 NH3﹤H2O,NH3 分子间有氢键,增加了分子间作用力
(3) 2H++2e-=H2↑ S2O82-+2H2O=H2O2+2HSO4-
【解析】
试题解析:X~R是元素周期表中的短周期元素,X能形成+7价的化合物,则X为Cl;Y是日常生活中常见金属,熔化时并不滴落,好象有一层膜兜着,则Y为Al;Z通常状况下能形成短周期中最稳定的双原子分子,则Z为N;W焰色反应为黄色,则W为Na;R最外层有二个未成对电子,无正价,则R为O。(1)基态氯原子核外有三个电子层,其中最高能层的能层符号是M;(2)Z是氮元素,其氢化物是NH3,电子式为: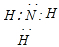 ;其中心原子氮原子的轨道杂化类型是SP3;元素Z是N、R是O,O的非金属性强于N,则气体氢化物的稳定性顺序是NH3﹤H2O;NH3易液化,原因是NH3 分子间有氢键,增加了分子间作用力;(4)电解KHSO4溶液时,阳极反应式是2HSO4--2e-=S2O82-+2H+,阴极氢离子放电生成氢气,阴极反应式是2H++2e-=H2↑;1mol S2O82-与水反应得到H2O2时转移了2mole-,S元素被还原为+6价,还生成SO42-,则该反应的离子方程式S2O82-+2H2O═H2O2+2HSO42-。
;其中心原子氮原子的轨道杂化类型是SP3;元素Z是N、R是O,O的非金属性强于N,则气体氢化物的稳定性顺序是NH3﹤H2O;NH3易液化,原因是NH3 分子间有氢键,增加了分子间作用力;(4)电解KHSO4溶液时,阳极反应式是2HSO4--2e-=S2O82-+2H+,阴极氢离子放电生成氢气,阴极反应式是2H++2e-=H2↑;1mol S2O82-与水反应得到H2O2时转移了2mole-,S元素被还原为+6价,还生成SO42-,则该反应的离子方程式S2O82-+2H2O═H2O2+2HSO42-。
考点:元素周期律与元素周期表


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源:2015届四川省2015届高三9月理综化学试卷(解析版) 题型:选择题
下列反应的离子方程式书写正确的是:
A.用硫氰化钾溶液检验Fe3+:Fe3++3SCN- = Fe(SCN)3↓
B.向海带灰浸出液中加入稀硫酸、双氧水:2I- + 2H+ + H2O2 = I2 + 2H2O
C.磨口玻璃试剂瓶被烧碱溶液腐蚀:SiO2+2Na++2OH- = Na2SiO3↓+H2O
D.NaHCO3溶液和少量Ba(OH)2溶液混合:HCO3- + OH-+ Ba2+ = H2O + BaCO3↓
查看答案和解析>>
科目:高中化学 来源:2015届四川省绵竹市高三上学期第二次月考化学试卷(解析版) 题型:选择题
某充电电池的原理如图所示,溶液中c(H+)=2.0mol?L﹣1,阴离子为SO42﹣,a、b均为惰性电极,充电时右槽溶液颜色由绿色变为紫色.下列对此电池叙述正确的是
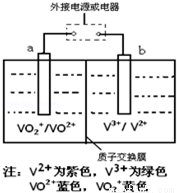
A.放电过程中,左槽溶液颜色由黄色变为蓝色
B.充电时,b极接直流电源正极,a极接直流电源负极
C.充电过程中,a极的反应式为:VO2++2H++e﹣=VO2++H2O
D.放电时,当转移1.0 mol电子时共有1.0 mol H+从左槽迁移进右槽
查看答案和解析>>
科目:高中化学 来源:2015届四川省高三(补习班)10月月考理综化学试卷(解析版) 题型:填空题
(12分)某无色透明溶液中可能大量存在Ag+、Mg2+、Cu2+、Fe3+、Na+中的几种,请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子是________。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是________ ,有关的离子方程式为________________________________。
(3)取(2)中的滤液,加入过量的稀氨水(NH3·H2O),出现白色沉淀,说明原溶液中肯定有________,有关的离子方程式为____________________________。
(4)原溶液可能大量存在的阴离子是下列的________。
A.Cl- B.NO3- C.CO32- D.OH-
查看答案和解析>>
科目:高中化学 来源:2015届四川省高三(补习班)10月月考理综化学试卷(解析版) 题型:选择题
下列关于药品的取用和保存,仪器选用正确的是
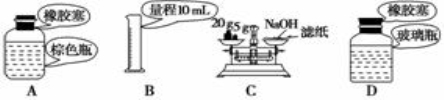
A.实验室中保存浓硝酸 B.准确量取9.50 mL稀硫酸
C.用托盘天平称量NaOH固体 D.实验室中保存Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源:2015届四川省成都高新区高三11月统一检测化学试卷(解析版) 题型:选择题
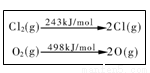
下列说法中正确的是
A.生成物总能量一定低于反应物总能量
B.同温同压下,H2(g)+Cl2(g)=2HCl(g) 在光照和点燃条件下的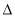 H不同
H不同
C.一定条件下,0.5 mol N2和1.5 mol H2置于某密闭容器中充分反应生成NH3气,放热19.3 kJ,其热化学方程式为N2(g)+3H2(g) 2NH3(g)
2NH3(g) 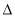 H =-38.6 kJ/mol
H =-38.6 kJ/mol
D.一定条件下4 HCl(g)+O2(g)=2Cl2(g)+2H2O(g) ,当1 molO2 反应放出115.6 kJ热量,键能如表所示,则断裂1 mol H-O键与断裂1 mol H-Cl键所需能量差为31.9 kJ
查看答案和解析>>
科目:高中化学 来源:2015届四川省成都高新区高三11月统一检测化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.在pH=1的溶液中:K+、Na+、SO42–、 IO3-、I-
B.在0.1 mol·L-1 Na2CO3溶液中:Al3+、K+、NO3-、SO42–
C.0.1 mol/L的NaNO3溶液:H+、Fe2+、Cl-、SO42-
D.在c( H+)/c(OH-)=10-12的溶液中:K+、Na+、ClO-、NO3-
查看答案和解析>>
科目:高中化学 来源:2015届吉林省长春外国语学校高三上学期期中理综化学试卷(解析版) 题型:选择题
在一密闭容器中充入一定量的N2和O2,在电火花作用下发生反应N2+O2  2NO,经测定前5 s用N2表示的反应速率为0.1 mol·L-1·s-1,则10 s末NO的浓度为
2NO,经测定前5 s用N2表示的反应速率为0.1 mol·L-1·s-1,则10 s末NO的浓度为
A.大于2 mol·L-1 B.2 mol·L-1
C.小于2 mol·L-1 D.不能确定
查看答案和解析>>
科目:高中化学 来源:2015届吉林省高三10月月考化学试卷(解析版) 题型:选择题
在氯化铁、氯化铜和盐酸的混合溶液中加入铁粉,待反应结束,所剩余的固体滤出后能被磁铁吸引,则反应后溶液中存在较多的阳离子是( )
A.Cu2+ B.Fe2+ C.Fe3+ D.H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com