
| A. | 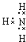 | B. | 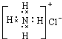 | ||
| C. | 氨水化学式:NH4OH | D. | NH3结构式: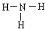 |
分析 A.氨气有3个氢原子和1个氮原子分别共用1对电子形成,氮原子还剩余1对孤对电子;
B.氯离子为阴离子,电子式中需要标出氯离子的最外层8个电子;
C.依据一水合氨化学式判断;
D.氨气是氮原子和氢原子之间通过共价单键形成的三角锥形结构.
解答 解:A.氨气有3个氢原子和1个氮原子分别共用1对电子形成,电子式为: ,故A错误;
,故A错误;
B.氯化铵是离子化合物,由氨根离子与氯离子构成,电子式为 ,故B错误;
,故B错误;
C.一水合氨化学式为NH3•H2O,故C错误;
D.氨气是氮原子和氢原子之间通过共价单键形成的三角锥形结构,结构式为: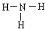 ,故D正确;
,故D正确;
故选:D.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及电子式结构式、化学式等知识,明确常见化学用语的书写原则为解答关键,有助于学生养成规范使用化学用语的习惯.


科目:高中化学 来源: 题型:选择题
| A. | 若2,2,3,3-四甲基戊烷由烯烃加成而来,则该烯烃的名称是2,2,3,3-四甲基-1--戊烯 | |
| B. | 在氯化银的沉淀溶解平衡体系中,加入蒸馏水,氯化银的Ksp增大 | |
| C. | 在氯化银的沉淀溶解平衡体系中,加入碘化钾固体,氯化银沉淀可转化为碘化银沉淀 | |
| D. | 在碳酸钙的沉淀溶解平衡体系中,加入稀盐酸,溶解平衡不移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
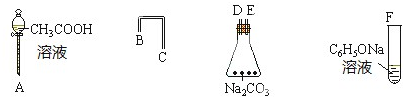

查看答案和解析>>
科目:高中化学 来源: 题型:推断题
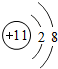 ;
;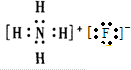 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
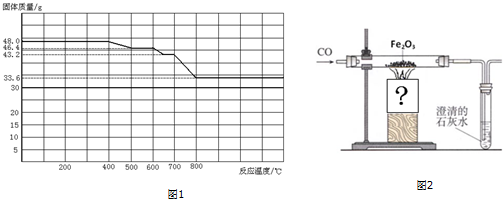
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 操作 | 现象 | 结论 |
| 取少量除尽Ag+后的溶液于试管中,加入KSCN溶液,振荡 | 变成血红色 | 存在Fe3+ |
| 取少量除尽Ag+后的溶液于试管中,加入K3[Fe(CN)6],振荡 | 产生蓝色沉淀 | 存在Fe2+ |
| 实验编号 | 操作 | 现象 |
| a | 加入足量氨水,振荡 | 黑色固体不溶解 |
| b | 加入足量稀硫酸,振荡 | 黑色固体溶解,并有气体产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 负极是铝失电子被氧化 | |
| B. | 电池工作时,电流由铝电极沿导线流向铂电极 | |
| C. | 以网状的铂为正极,可增大与氧气的接触面积 | |
| D. | 该电池通常只需更换铝板就可继续使用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com