
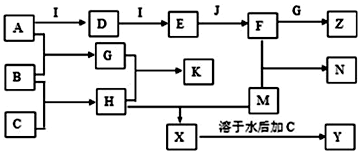
分析 已知A、B、C、D、E、G、H、I均为气体,A、B、C、I、M为单质,G可使湿润红色石蕊试纸变蓝,则G为NH3,G和H相遇时产生白烟,则H为HCl,则K为NH4Cl,B和C能生成H,则C为Cl2,B为H2,A为N2,J为常见的液态物质,则J为H2O,根据转化关系可知,I为O2,D为NO,E为NO2,F为HNO3,Z为NH4NO3,M为常见金属,M能与盐酸反应后又与氯气反应,所以M为Fe,所以X为FeCl2,Y为FeCl3,以此解答该题.
解答 解:(1)由以上分析可知A为,故答案为:N2;
(2)①实验室用氯化铵制取氨气的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$ CaCl2+2NH3↑+2H2O,
故答案为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;
②实验室检验气体氨气是否收集满的方法是用湿润的红色石蕊试纸靠近于集气瓶口,如果红色石蕊试纸变蓝,则说明收集满,
故答案为:用湿润的红色石蕊试纸靠近于集气瓶口,如果红色石蕊试纸变蓝,则说明收集满;
③氯化氢遇到氨气生成氯化铵,出现白烟,反应的化学方程式为NH3+HCl═NH4Cl,
故答案为:NH3+HCl═NH4Cl;
(3)①F为HNO3,F的浓溶液与木炭反应的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ CO2↑+4NO2↑+2H2O,
故答案为:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O;
②工业浓硝酸溶液呈黄色,是因为浓硝酸分解产生二氧化氮,反应方程式为:4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ 4NO2↑+O2↑+2H2O,若要消除黄色可向其中通入一定量的氧气,
故答案为:4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$4NO2↑+O2↑+2H2O;氧气.
点评 本题为框图型物质推断题,为高考常见题型,侧重考查学生的分析能力,完成此类题目,可以依据题干提供的信息,根据物质的性质结合框图,找准解题的突破口,直接得出物质的化学式,然后顺推或逆推或由两边向中间推得出其他物质的化学式.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KNO3溶液:Fe2+、I-、SO42-、H+ | |
| B. | 含大量Al3+的溶液中:Cu2+、Na+、SO42-、NO3- | |
| C. | 由水电离出的c(H+)=1.0×10-12的溶液中:Ba2+、K+、Cl-、HCO3- | |
| D. | 使甲基橙呈红色的溶液:Na+、K+、SiO32-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2通入Ba(NO3)2溶液中无沉淀生成,推出SO2通入Ba(NO3)2溶液中无沉淀生成 | |
| B. | Fe3Cl8可以改写为FeCl2•2FeCl3,推出Fe3I8可以改写为FeI2•2FeI3 | |
| C. | NH3的沸点高于PH3,推出CH4沸点高于SiH4 | |
| D. | H2SO4为强酸,推出HC1O4为强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡是能量达到活化能的分子发生的碰撞均为有效碰撞 | |
| B. | 熵增大的反应都是自发反应,熵减少的反应都不能进行 | |
| C. | 升高温度,可逆反应的正反应速率和逆反应速率都一定增大 | |
| D. | 使用催化剂可以增加反应物分子的能量,从而增大反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5 mol Al与足量盐酸反应转移电子数为NA | |
| B. | 标准状况下,22.4 L氨气与22.4 L氮气所含原子数均为2 NA | |
| C. | 7.8gNa2O2所含的离子数为0.3NA | |
| D. | 11.2LCl2完全溶于NaOH溶液,电子转移数为0.5 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定条件下足量的Fe粉与浓硫酸反应,转移电子数一定为3NA | |
| B. | 在标准状况下,1L pH=13的NaOH溶液中,含有0.1NA个OH- | |
| C. | 常温常压下,11.2 L Cl2中含有的分子数为3.01×l023个 | |
| D. | 常温下7g环丙烷和乙烯组成的混合气体中含有氢原子的数目为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com