
����Ŀ�����н�����ʵ�ķ���ʽ��ȷ���ǣ� ��
A.���Ȼ�����Һ������ʵ�飬���ݷ��⣺NaCl ![]() Na++Cl��
Na++Cl��
B.�����������������������Fe��OH��3+3H+�TFe3++3H2O
C.ʯ��ˮ����Ư�ŵġ���Ĥ�����ô����ܽ⣺CaCO3+2H+�TCa2++H2O+CO2��
D.������������Һ�еμ�����������Һ���պ�Ϊ���ԣ�2H++SO42��+Ba2++2OH���TBaSO4��+2H2O
���𰸡�D
���������⣺A�����Ȼ�����Һ������ʵ�飬���ݷ��⣬��������ΪNaCl=Na++Cl�� �� ��A����
B������������������������е����ӷ�ӦΪ2Fe��OH��3+2I��+6H+�T2Fe2++I2+6H2O����B����
C��ʯ��ˮ����Ư�ŵġ���Ĥ�����ô����ܽ�����ӷ�ӦΪCaCO3+2CH3COOH�T2CH3COO��+Ca2++H2O+CO2������C����
D��������������Һ�еμ�����������Һ���պ�Ϊ���Ե����ӷ�ӦΪ2H++SO42��+Ba2++2OH���TBaSO4��+2H2O����D��ȷ��
��ѡD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£��͵��ռ���Һ�з���һ�����Ľ����ƣ���ַ�Ӧ��ָ���ԭ�����¶ȣ�����˵����ȷ����
A. ��Һ��Na+��Ŀ���٣���H2�ų� B. ��Һ��OH-Ũ��������H2�ų�
C. ��Һ��Na+Ũ��������H2�ų� D. ��Һ��OH-Ũ��������O2�ų�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£����ݻ�Ϊ2L���ܱ�������ͨ���������巢����ѧ��Ӧ����Ӧ�и����ʵ����仯��ͼ��ʾ���Ը÷�Ӧ���ƶϺ������ǣ� �� 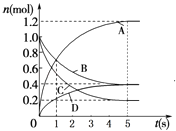
A.�÷�Ӧ�Ļ�ѧ����ʽΪ6A+2 D3B+4C
B.��Ӧ���е�1 sʱ��v��A��=v��B��
C.��Ӧ���е�5 sʱ��B��ƽ����Ӧ����Ϊ0.06mol/��Ls��
D.��Ӧ���е�5 sʱ��v��A��=v��B��=v��C��=v��D��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����100��ʱ����0.40mol NO2�������2L���ܱ������У��������·�Ӧ��2NO2��g��N2O4��g����H��0����ⷴӦ���������ݣ�����˵����ȷ���ǣ� ��
ʱ��/s | 0 | 20 | 40 | 60 | 80 |
n��NO2��/mol | 0.40 | n1 | 0.26 | n3 | n4 |
n��N2O4��/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
A.0��20 s�ڣ�v��NO2��=0.005 mol?L��1?s��1
B.59 sʱ��c��NO2��һ������0.12 mol?L��1
C.��������ʼʱ����NO2��������0.80 mol����÷�Ӧ��ƽ�ⳣ��K�� ![]()
D.��������Ӧ��120��ʱ���У���Ӧ��80 sʱ��n��N2O4����0.08 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ�����S2Cl2���ǹ㷺������ҵ����������ӽṹ��ͼ��ʾ��������S2Cl2��һ�ֳȻ�ɫ��Һ�壬��ˮ��ˮ�⣬��������ʹƷ����ɫ�����壮
����˵��������ǣ� ��
A.S2Cl2�ĽṹʽΪCl��S��S��Cl
B.S2Cl2Ϊ���м��Լ��ͷǼ��Լ��ķǼ��Է���
C.S2Br2��S2Cl2�ṹ���ƣ����Ӽ���������S2Br2��S2Cl2
D.S2Cl2��H2O��Ӧ�Ļ�ѧ����ʽ����Ϊ��2S2Cl2+2H2O�TSO2��+3S��+4HCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�ϳɰ���Ӧ��N2+3H22NH3��һ�����ȵĿ��淴Ӧ����Ӧ�����Ǹ��¡���ѹ��������Ҫ���ʵĴ�������֪�γ�1mol H��H����1mol N��H����1mol N��N���ų������ֱ�Ϊ436kJ��391kJ��946kJ����
��1����1mol N2��ȫ��Ӧ����NH3��������ա��ų���������kJ��
��2�������1mol N2��3mol H2��ϣ�ʹ���ַ�Ӧ���ų���������С��������ֵ����ԭ����
��3��ʵ����ģ�ҵ�ϳɰ�ʱ�����ݻ�Ϊ2L���ܱ������ڣ���Ӧ����10min������10mol NH3 �� ����N2��ʾ�Ļ�ѧ��Ӧ����Ϊ ��
��4��һ�������£����ϳɰ��ķ�Ӧ�ﵽ��ѧƽ��ʱ������˵����ȷ���� �� a������Ӧ���ʺ��淴Ӧ�������
b������Ӧ��������淴Ӧ����Ϊ0
c��N2��ת���ʴﵽ���ֵ
d��N2��H2��Ũ�����
e��N2��H2��NH3������������
f����Ӧ�ﵽ�����
��5�����ĸ���ͬ�����У���ͬ�����½��кϳɰ���Ӧ����������ͬʱ���ڲⶨ�Ľ�����жϸ÷�Ӧ�������ɴ�С��˳�������ñ����д����
A.V��NH3��=0.5molL��1��min��1
B.V��H2��=0.3molL��1��min��1
C.V��N2��=0.2molL��1��min��1
D.V��H2��=0.01molL��1��s��1 ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ñ�����ζ�����������Һ��������ָʾ���������в�����ȷ����
A.��ƿ������ˮϴ�Ӻ���������������Һ��ϴ
B.�ζ���������ˮϴ�Ӻ�װ���������еζ�
C.�ζ�ʱ����ҡ����ƿ�߹۲�ƿ����Һ����ɫ�仯
D.���ζ�����Һ�ɻ�ɫ��Ϊ��ɫʱ����Ϊ�ζ��յ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ϳɰ�������ع�ҵ�У��������ʼ��ת����ϵ��ͼ������˵������ȷ���ǣ� ��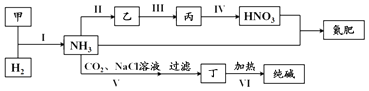
A.�ס��ҡ������������ж����е�Ԫ��
B.��ӦII��III�͢����������ֱ��������������Ͷ�����������һ��
C.����������ˮ֮�䷴Ӧ���������NO��VI�IJ���NO�������������б��ٴ�����
D.�����Ͷ�����̼ͨ���Ȼ�����Һ���������ܽ�Ƚ�С��̼�����ƾ��壬������Ӧ��NH3+CO2+H2O+NaCl�TNaHCO3��+NH4Cl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����4���ƵĻ����W��X��Y��Z������֮��������¹�ϵ����W ![]() X+CO2+H2O��
X+CO2+H2O��
��Z+CO2��X+O2��
��Z+H2O��Y+O2����
��X+Ca��OH��2��Y+CaCO3����
���⣺
��1����X�������� �� Z���������Ӹ���֮��Ϊ
��2��д����Ӧ�����ӷ���ʽ��
��3��д��Ca��OH��2�����W��Ӧ��ѧ����ʽ��
��4����������¶Ȳ�����ܱ������У�����һ������Z��һ������CO2��ַ�Ӧ����÷�Ӧǰ��ѹǿ֮��Ϊ5��4����Ӧ��������CO2��O2���ʵ���֮��Ϊ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com