
【题目】T℃时,向10L容积不变的密闭容器中加入1.0molNH2COONH4,发生反应NH2COONH4(s)![]() CO2(g)+2NH3(g) ΔH>0。5min达到平衡时,测得容器中NH2COONH4(s)的物质的量为0.2mol。下列说法正确的是
CO2(g)+2NH3(g) ΔH>0。5min达到平衡时,测得容器中NH2COONH4(s)的物质的量为0.2mol。下列说法正确的是
A. 0~5min内,v(CO2)=0.16mol·L-1·min-1
B. 氨气体积分数不变时,该反应一定达到平衡状态
C. 平衡后,缩小容器容积,重新建立平衡时,c(CO2)增大
D. 其他条件不变,若将原容器改为绝热容器,则达到平衡时,NH2COONH4的转化率小于80%
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】现有几种物质①NH4Cl ②Na2S ③Na2O2 ④H2S ⑤CO2 ⑥MgCl2回答问题:
(1)①~⑥中,仅含离子键的是____,既有离子键又有共价键的是______,(以上用数字代码回答)
(2)写出①NH4Cl ③Na2O2 ⑤CO2三种物质的电子式①______③______⑤________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,反应4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g) △H =-a kJ·mol-1,在5 L密闭容器中进行,10 s时达到平衡,水蒸气的物质的量增加了0.6 mol,则下列说法正确的是( )
4NO(g)+6H2O(g) △H =-a kJ·mol-1,在5 L密闭容器中进行,10 s时达到平衡,水蒸气的物质的量增加了0.6 mol,则下列说法正确的是( )
A.第10s时,H2O的反应速率为0.012 mol·Lˉ1·sˉ1
B.10s内,NH3的平均反应速率为0.48 mol·Lˉ1·minˉ1
C.10s内,反应放出的热量为a kJ
D.这10s内,O2的反应速率逐渐减小,NO的反应速率逐渐增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。下列对该燃料电池说法正确的是
A.在熔融电解质中,O2-由负极移向正极
B.通入空气的一极是正极,电极反应为:O2+2H2O+4e-=4OH-
C.通入丁烷的一极是负极,电极反应为:C4H10+26e-+13O2-=4CO2+5H2O
D.在电池反应中,每消耗1mol氧气,理论上能生成标准状况下CO2气体![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于可逆反应的是( )
A. Fe + CuCl2﹦FeCl2 + Cu B. 2 Na + 2H2O = 2NaOH + H2↑
C. 2H2 + O2![]() 2H2O D. H2+I2
2H2O D. H2+I2 ![]() 2HI
2HI
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某试液中只可能含有K+、NH4+、Fe2+、Al3+、Clˉ、CO![]() 、SO
、SO![]() 、NO3-中的若干种离子,离子浓度均为0.1 mol·Lˉ1,某同学进行如下实验:下列说法正确的是( )
、NO3-中的若干种离子,离子浓度均为0.1 mol·Lˉ1,某同学进行如下实验:下列说法正确的是( )
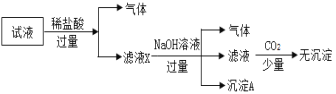
A.原试液中可能含有CO![]() 、K+、NH4+
、K+、NH4+
B.无法确定沉淀A的成分
C.无法确定原试液中有Al3+、K +、Clˉ
D.原溶液中一定存在的离子为NH、Fe2+、SO![]() 、NO3-
、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关金属铝及其化合物的叙述正确的是( )
A.铝在常温下不能与氧气反应
B.铝不能与氯气反应
C.氧化铝只能与酸反应,不能与碱反应
D.铝既能溶于酸,又能溶于强碱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com