
下列关于pH变化的判断正确的是( )
A.温度升,Na2CO3溶液pH减小
B.温度升高,纯水pH增大
C.新制氯水经光照一段时间后,溶液pH减小
D.氢氧化钠溶液久置于空气中,溶液pH变大
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
在反应2SO2+O2
 2SO3中,有a mol SO2和b mol O2参加反应,达到化学平衡状态时有c mol SO3生成,则SO2在平衡混合物中的体积分数为( )
2SO3中,有a mol SO2和b mol O2参加反应,达到化学平衡状态时有c mol SO3生成,则SO2在平衡混合物中的体积分数为( )
A. ×100% B.
×100% B.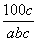 ×100%
×100%
C. ×100% D.
×100% D.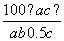 %
%
查看答案和解析>>
科目:高中化学 来源: 题型:
CO和NO都是汽车尾气中的有害物质,它们之间能缓慢地发生如下反应:2NO(g)+2CO(g)N2(g)+2CO2(g) ΔH<0,现利用此反应,拟设计一种环保装置,用来消除汽车尾气对大气的污染,下列设计方案可以提高尾气处理效果的是 ( )。
①选用适当的催化剂 ②提高装置温度 ③降低装置的压强 ④装置中放入碱石灰
A.①③ B.②④
C.①④ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、M都是中学教材常见元素,下列对两个离子反应通式的推断中,其中正确的是( )
(甲) XO3n-+Xn- + H+ →X单质+ H2O(未配平); (乙)Mm++mOH-=M(OH)m↓
①若n=1,则XO3n-中X元素为+5价,X位于周期表第ⅤA族
②若n=2,则X最高价氧化物的水化物可能与它的氢化物反应
③若m=1,则M(NO3)m溶液和氨水互滴时的现象可能不同
④若m=2,则在空气中蒸干、灼烧MSO4溶液一定能得到MSO4
⑤若m=3,则MCl3与足量氢氧化钠溶液反应一定生成M(OH)m
A.①③ B. ②③ C. ①② D. ④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ.据有关资料显示,海底有大量的天然气水合物,可满足人类1000年的能源需要。天然气水合物是一种晶体,晶体中平均每46个水分子构建成8个笼,每个笼可容纳1个CH4分子或1个游离H2O分子。根据上述信息,完成下面两题:
(1)下列关于天然气水合物中两种分子描述正确的是
A.两种都是极性分子 B.两种都是非极性分子
C.H2O是极性分子,CH4是非极性分子 D.其中氧原子和碳原子的杂化方式均为sp3
E.其中氧原子和碳原子的杂化方式分别为sp2和sp3
(2)晶体中每8个笼只有6个容纳了CH4分子,另外2个笼被游离H2O分子填充,则天然气水合物的平均组成可表示为
II.(1)兰聚氰胺分子的结构简式如图所示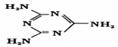 ,则其中氮原子轨道杂化类型是 ,l mol三聚氰胺分子中含 mol
,则其中氮原子轨道杂化类型是 ,l mol三聚氰胺分子中含 mol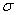 键。
键。
(2)某元素位于第四周期VIII族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的M层电子排布式为____ 。
 (3)过渡金属配合物Ni( CO)n的中心原子价电子数与配体提供电子总数之和为18,则n=____ 。
(3)过渡金属配合物Ni( CO)n的中心原子价电子数与配体提供电子总数之和为18,则n=____ 。
(4)碳化硅的晶胞结构(如右图)与金刚石类
似(其中“●”为碳原子,“○”为硅原子)。
图中“●”点构成的堆积方式与下列图式
中 所表示的堆积方式相同。

(5)碳化硅的结构中,设晶胞边长为a cm,碳原子直径为b cm,硅原子直径为c cm,则该晶胞的空间利用率为 (用含a、b、c的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
对于常温下pH为1的硝酸溶液,下列叙述正确的是( )
A.该溶液1 mL稀释至100 mL后,pH大于3
B.向该溶液中加入等体积、pH为13的氢氧化钡溶液恰好完全中和
C.该溶液中硝酸电离出的[H+]与水电离出的[H+]的比值为10-12
D.该溶液中水电离出的[H+]是pH为3的硝酸中水电离出的[H+]的100倍
查看答案和解析>>
科目:高中化学 来源: 题型:
汽车尾气中CO、NOx 以及燃煤废弃中的SO2都是大气污染物,对它们的治理具有重要意义。
Ⅰ.CH4(g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g) △H1= —574 kJ·mol- 1 .
CH4(g) + 4NO(g) = 2N2(g)+CO2(g)+2H2O(g) △H2= 一1160 kJ·mol- 1
(1)甲烷直接将NO2还原为N2的热化学方程式为 ;
Ⅱ.吸收SO2和NO,获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素):

(2)装置Ⅱ中,酸性条件下,NO被Ce 4+ 氧化的产物主要是NO3- 、NO2- ,写出只生成NO3- 的离子方程式 ;
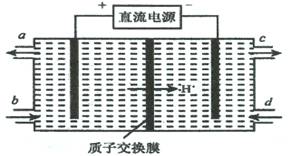
(3)装置Ⅲ的作用之一是再生Ce4+,其原理如下图所示。
①生成的Ce4+ 从电解槽的 (填字母序号)口流出;
②生成S2O42 - 的电极反应式为 ;
(4)已知进入装置Ⅳ的溶液中,NO2- 的浓度为a g·L- 1 ,要
使1m3该溶液中的NO2- 完全转化为NH4NO3,至少需向装置Ⅳ
中通入标准状况下的O2 L。(用含a代数式表示,计算结果保留整数)

查看答案和解析>>
科目:高中化学 来源: 题型:
.向含有一定量盐酸和少量MgSO4的混合溶液中逐滴加入Ba(OH)2溶液,产生沉淀的质量m与加入Ba(OH)2的物质的量n之间的关系如图所示,下列说法正确的是

A.  时的沉淀成分为BaSO4与Mg(OH)2
时的沉淀成分为BaSO4与Mg(OH)2
B.  时发生的离子反应为H++OH-=H2O
时发生的离子反应为H++OH-=H2O
C. c点时的溶液中
D. 原混合溶液中:n(HCl)=2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列每组中各有三对物质,它们都能用分液漏斗分离的是( )
A.乙酸乙酯和水、酒精和水、苯酚和水
B.二溴乙烷和水、溴苯和水、硝基苯和水
C.甘油和水、乙醛和水、乙酸和乙醇
D.油酸和水、甲苯和水、己烷和苯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com