
某学生鉴定甲盐的流程如图所示,下列说法正确的是
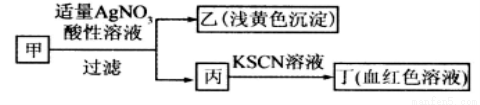
A.如果甲中含有S2-,则乙是硫磺沉淀
B.如果乙是AgCl沉淀,那么甲是FeCl3
C.丙中肯定含有Fe3+,所以甲是FeBr2
D.甲中含有铁元素,可能显示+2或者+3价
科目:高中化学 来源:2016届山东省济宁市高三上学期期中考试化学试卷(解析版) 题型:实验题
某实验小组利用氯气与金属铁反应制备无水三氯化铁,经查阅资料得知:无水FeCl3在空气中易潮解,加热到100℃左右时易升华。下图是两个学生设计的实验装置,左边的反应装置相同,而右边的产品收集装置不同,分别如(I)和(Ⅱ)所示,试回答:

(1)B中反应的离子方程式为__ __;
(2)实验中a与b两个酒精灯应先点燃 ,目的是 ;
(3)收集装置(Ⅰ)的主要缺点是: ;装置(Ⅱ)也有缺点,必须采取的改进措施是:___ _。
(4)b酒精灯加热后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管D右端,要使沉积的FeCl3 进入收集器,操作是 。
(5)实验中还缺少一个除杂装置,目的是除去 ;应选择 做除杂剂。
A.饱和NaHCO3 B.水 C.饱和食盐水 D.NaOH溶液
查看答案和解析>>
科目:高中化学 来源:2016届辽宁师范大学附属中学高三上学期期中考试化学试卷(解析版) 题型:选择题
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为:
CH3CH2OH-4e-+H2O=CH3COOH+4H+。下列有关说法不正确的是( )
A.检测时,电解质溶液中的H+向正极移动
B.若溶液中有0.4 mol电子通过,则在标准状况下消耗4.48 L氧气
C.电池反应的化学方程式为:CH3CH2OH+O2==CH3COOH+H2O
D.正极上发生的反应为:O2+4e-+4H+=2H2O
查看答案和解析>>
科目:高中化学 来源:2016届江西省南昌市高三上学期第四次考试化学试卷(解析版) 题型:选择题
下列两种方案制备氢氧化铝:
方案一:2.7g Al 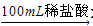 X溶液
X溶液 Al(OH)3沉淀
Al(OH)3沉淀
方案二:2.7g Al 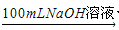 Y溶液
Y溶液 Al(OH)3沉淀
Al(OH)3沉淀
已知所用的稀盐酸与NaOH溶液均为3mol/L.图是向X溶液与Y溶液中分别加入NaOH溶液或稀盐酸时产生沉淀的质量与加入溶液体积之间的关系.相关说法正确的是

A.a曲线表示的是向Y溶液中加入NaOH溶液
B.方案二比方案一生成更多的气体
C.在M点时,两种方案中所得溶液的溶质质量分数相同
D.M点以后,a、b两条曲线将重合为一条
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三上学期期中考试化学试卷(解析版) 题型:选择题
CuO、Fe粉、Fe3O4的混合物中,加一定量稀硫酸,当反应停止后,滤出不溶物,并向滤液中插入一枚铁钉,片刻后.取出铁钉,观察现象。以下结论中正确的是( )
A.若铁钉部分溶解,则滤液中一定含Fe2(SO4)3
B.若铁钉完全溶解,则滤液中一定含CuSO4
C.若铁钉表面有红色物质生成,则不溶物中一定不含Fe
D.若铁钉无变化,则不溶物中一定含Fe
查看答案和解析>>
科目:高中化学 来源:2016届江西上高第二中学高三12月月考理科综合化学试卷(解析版) 题型:选择题
化学与人类生活密切相关,下列与化学有关的说法正确的是( )
A.温室效应是当今世界面临的环境问题,使温室效应增强的气体只有二氧化碳
B.侯氏制碱法的工艺过程中主要应用了物质熔沸点的差异
C.家庭用的“84”消毒液与洁厕灵不能同时混合使用,否则会发生中毒事故
D.实验室里熔化氢氧化钠时,可选用石英坩埚和铁坩埚
查看答案和解析>>
科目:高中化学 来源:2016届贵州遵义航天高中高三上学期第三次模拟理综化学试卷(解析版) 题型:简答题
1913年,德国化学家哈伯实现了合成氨的工业化生产,被称作解救世界粮食危机的化学天才。现将lmolN2和3molH2投入1L的密闭容器,在一定条件下,利用如下反应模拟哈伯合成氨的工业化生产:N2(g)+3H2(g) 2NH3(g) △H<0
2NH3(g) △H<0
当改变某一外界条件(温度或压强)时,NH3的体积分数ψ(NH3)变化趋势如下图所示。

回答下列问题:
(1)已知:①NH3(g)  NH3(g) △H1
NH3(g) △H1
②N2(g)+3H2(g) 2NH3(l) △H2
2NH3(l) △H2
则反应N2(g)+3H2(g) 2NH3(g)的△H= (用含△H1、△H2的代数式表示)。
2NH3(g)的△H= (用含△H1、△H2的代数式表示)。
(2)合成氨的平衡常数表达式为____ ,平衡时,M点NH3的体积分数为10%,则N2的转化率为 (保留两位有效数字)。
(3)X轴上a点的数值比b点 (填“大”或“小”)。上图中, Y轴表示 (填“温度”或“压强”),判断的理由是 。
(4)若将1mol N2和3mol H2分别投入起始容积为1L的密闭容器中,实验条件和平衡时的相关数据如下表所示:
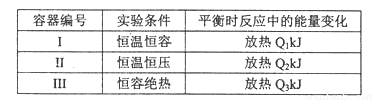
下列判断正确的是____。
A.放出热量:Ql< Q2< △Hl B. N2的转化率:I> III
C.平衡常数:II >I D.达平衡时氨气的体积分数:I>II
(5)常温下,向VmL amoI.L-l的稀硫酸溶液中滴加等体积bmol.L-l 的氨水,恰好使混合溶液呈中性,此时溶液中c(NH4+)__c(SO42-)(填“>”、“<”或“=”)。
(6)利用氨气设计一种环保燃料电池,一极通入氨气,另一极通入空气,电解质是掺杂氧化钇(Y203)的氧化锆(ZrO2)晶体,它在熔融状态下能传导O2-。写出负极的电极反应式 。
查看答案和解析>>
科目:高中化学 来源:2015-2016浙江宁波效实中学高一上期中考试化学试卷(解析版) 题型:选择题
设NA 表示阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,0.1 mol Cl2 溶于水,转移的电子数目为0.1NA
B.常温常压下,18 g H2O 中含有的原子总数为3NA
C.标准状况下,11.2 L 乙醇中含有的分子数目为0.5NA
D.常温常压下,2.24 L CO 和CO2 混合气体中含有的碳原子数目为0.1NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com