
【题目】N2的结构可以表示为![]() ,CO的结构可以表示为
,CO的结构可以表示为![]() ,其中椭圆框表示π键,下列说法不正确的是( )
,其中椭圆框表示π键,下列说法不正确的是( )
A. N2分子与CO分子中都含有三键
B. N2分子与CO分子中π键并不完全相同
C. N2分子与CO分子互为等电子体
D. N2分子与CO分子的化学性质相同
【答案】D
【解析】
由题意可知N2分子中N原子之间、CO分子中C、O原子之间均通过2个π键,一个σ键,即三键结合,其中,CO分子中1个π键由O原子单方面提供孤电子对,C原子提供空轨道通过配位键形成。
A项、根据图象知,氮气和CO都含有两个π键和一个σ键,N2分子与CO分子中都含有三键,故A正确;
B项、氮气中π键由每个N原子各提供一个电子形成,而CO分子中其中一个π键由O原子提供1对电子形成属于配位键,故B正确;
C项、N2分子与CO分子中原子总数相同、价电子总数也相同,二者互为等电子体,故C正确;
D项、N2分子在空气中不燃烧,CO分子在空气中燃烧,所以两种分子的化学性质不相同,故D错误。
故选D。


科目:高中化学 来源: 题型:
【题目】为分析某盐的成分, 做了如下实验:
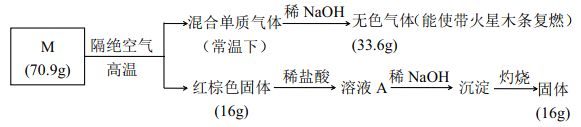
请回答:
(1)盐 M 的化学式是_________;
(2)被 NaOH 吸收的气体的电子式____________;
(3)向溶液 A 中通入H2S 气体, 有淡黄色沉淀产生, 写出反应的离子方程式________ (不考虑空气的影响)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 是一种高效安全消毒剂,常温下
是一种高效安全消毒剂,常温下![]() 为红黄色有刺激性气味气体,其熔点为-59.5℃,沸点为11.0℃,能溶于水但不与水反应,遇热水缓慢水解。某研究性学习小组欲制备
为红黄色有刺激性气味气体,其熔点为-59.5℃,沸点为11.0℃,能溶于水但不与水反应,遇热水缓慢水解。某研究性学习小组欲制备![]() 水溶液并检验其性质。
水溶液并检验其性质。
Ⅰ.二氧化氯水溶液制备。

在圆底烧瓶中先放入![]() 固体和
固体和![]() ,然后再加入5mL稀硫酸,用磁力搅拌棒搅拌(如图),将烧瓶放在热水浴中,保持60℃~80℃,至B中广口瓶内呈深红黄色时停止加热。回答下列问题:
,然后再加入5mL稀硫酸,用磁力搅拌棒搅拌(如图),将烧瓶放在热水浴中,保持60℃~80℃,至B中广口瓶内呈深红黄色时停止加热。回答下列问题:
(1)装置A用水浴加热的优点是_________;装置A中水浴温度不低于60℃,其原因是_______________。
(2)装置A中反应生成![]() 及
及![]() 等产物的化学方程式为_____________________;
等产物的化学方程式为_____________________;
(3)装置B的水中需放入冰块的目的是__________________;已知![]() 缓慢水解生成的含氯化合物只有
缓慢水解生成的含氯化合物只有![]() 和
和![]() ,且物质的量之比为2:1,则该反应的化学方程式为____________;装置C中的
,且物质的量之比为2:1,则该反应的化学方程式为____________;装置C中的![]() 溶液吸收尾气中的
溶液吸收尾气中的![]() ,生成物质的量之比为的1:1的两种盐,一种为
,生成物质的量之比为的1:1的两种盐,一种为![]() ,另一种为_________________。
,另一种为_________________。
Ⅱ.![]() 的含量测定
的含量测定
步骤1:量取![]() 溶液
溶液![]() ,稀释成
,稀释成![]() 试样;量取
试样;量取![]() 试样加入到锥形瓶中;
试样加入到锥形瓶中;
步骤2:调节试样的![]() ,加入足量的
,加入足量的![]() 晶体,振荡后,静置片刻;
晶体,振荡后,静置片刻;
步骤3:加入指示剂,用![]() 溶液滴定至终点,消耗
溶液滴定至终点,消耗![]() 溶液
溶液![]() 。
。
(4)已知:![]() ,
,![]() ,原
,原![]() 溶液的浓度为_____
溶液的浓度为_____![]() (用含字母的代数式表示),如果滴定速度过慢,会使计算出的数值______(填“偏大”、“偏小”或“不变”)。
(用含字母的代数式表示),如果滴定速度过慢,会使计算出的数值______(填“偏大”、“偏小”或“不变”)。
Ⅲ.设计实验验证![]() 的氧化性
的氧化性
(5)取适量![]() 水溶液加入
水溶液加入![]() 溶液中,振荡,得无色溶液。欲检验
溶液中,振荡,得无色溶液。欲检验![]() 的氧化产物,还需要用到的试剂是____________。
的氧化产物,还需要用到的试剂是____________。
(6)证明![]() 的氧化性比
的氧化性比![]() 强的方案是__________________________________。
强的方案是__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.已知:R-CH=CH-O-R′![]() R-CH2CHO + R′OH
R-CH2CHO + R′OH
(烃基烯基醚)
烃基烯基醚A的相对分子质量(Mr)为176,分子中碳氢原子数目比为3∶4 。与A相关的反应如下:
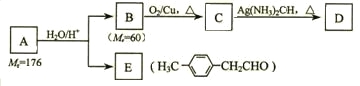
请回答下列问题:
⑴ A的分子式为_________________。
⑵ B的名称是__________;A的结构简式为_______________。
⑶写出C → D反应的化学方程式:_____________________________。
⑷写出两种同时符合下列条件的E的同分异构体的结构简式:
①属于芳香醛; ②苯环上有两种不同环境的氢原子。
_________________________、________________________。
Ⅱ.由E转化为对甲基苯乙炔(![]() )的一条路线如下:
)的一条路线如下:

⑸写出G的结构简式:___________________________。
⑹写出①-④步反应所加试剂、反应条件和①-③步反应类型:____________
序号 | 所加试剂及反应条件 | 反应类型 |
① | ||
② | ||
③ | ||
④ | —— |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NA是阿伏加德罗常数的值,下列说法错误的是( )
A.3g3He含有的中子数为1NA
B.48g正丁烷和10g异丁烷的混合物中共价键数目为13NA
C.在标准状况下,22.4LNH3被O2完全氧化为NO时,转移电子的数目为5NA
D.一定条件下,6.4g铜与过量的硫反应,转移电子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校研究性学习小组的同学进行了以下化学实验:将金属钙置于空气中燃烧,然后向所得固体产物中加入一定量蒸馏水,此过程中反应放出大量的热,并且放出有臭味的气体。
(1)甲同学提出:运用类比学习的思想,Ca与Mg位于同一主族,化学性质具有一定的相似性。请写出Ca在空气中燃烧发生反应的化学方程式___________________。
(2)乙同学提出:Ca的性质比Na活泼,在空气中燃烧还应有CaO2生成,请写出燃烧后固体产物与水反应放出气体的化学方程式____________________。
(3)丙同学提出用实验的方法探究放出臭味气体的成分:
(查阅资料)
1.CaO2遇水反应生成H2O2,H2O2可能会分解产生一定量的O3。
2.碘量法是最常用的臭氧测定方法,其原理为强氧化剂臭氧(O3)与碘化钾(KI)水溶液反应生成游离碘(I2),臭氧转化为氧气。反应式为O3+2KI+H2O=O2+I2+2KOH。
(提出假设)
假设1:该臭味气体只有NH3;
假设2:该臭味气体只有________;
假设3:该臭味气体含有________。
(设计方案 进行实验探究)
(4)该小组同学设计如下实验方案,并进行实验,验证上述假设。请完成相关的实验操作步骤、预期现象及结论(仪器自选)。
限选实验试剂:红色石蕊试纸、蓝色石蕊试纸、pH试纸、淀粉-KI溶液、蒸馏水。
实验操作 | 预期现象与结论 |
取少量反应后固体于试管中,______ | _____________ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH=1的两种酸溶液A、B各1mL,分别加水稀释到1000mL,其pH与溶液体积(V)的关系如图所示,下列说法不正确的是

A. A、B两种酸溶液的物质的量浓度一定相等
B. 稀释后,A酸溶液的酸性比B酸溶液的酸性弱
C. 若a=4,则A是强酸,B是弱酸
D. 若1<a<4,则A、B都是弱酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)家用液化气的主要成分之一是丁烷,当10kg丁烷完全燃烧并生成二氧化碳和液态水时,放出热量为5×105kJ,试写出表示丁烷燃烧热的热化学方程式:_____________________________________________________
(2)已知:C(s)+O2(g)===CO2(g);ΔH=-393.5 kJ/mol;2H2(g)+O2(g)===2H2O(g);ΔH=-483.6 kJ/mol,现有0.2 mol的炭粉和氢气组成的悬浮气,因混合物在氧气中完全燃烧,共放出63.53 kJ热量,则混合物中C与H2的物质的量之比为________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。

根据判断出的元素回答问题:
上述元素可组成盐R:zx4f(gd4)2。向盛有10mL 1mol·L-1R溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积的变化示意图如下:

(1)R溶液中,离子浓度由大到小的顺序是___________________________________
(2)写出m点反应的离子方程式:__________________________________________。
(3)若在R溶液中改加20mL 1.2mol·L-1 Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为________ mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com