
| A. | 标准状况下,33.6 L H2O含有的H2O分子数为1.5 NA | |
| B. | 常温常压下,32g O2和28 g N2所含分子个数比为1:1 | |
| C. | 0.5 mol/L AlCl3溶液中含有的Cl-数为1.5 NA | |
| D. | 1 mol Na2O2与足量CO2完全反应转移的电子数目为2 NA |
分析 A、标况下水为液态;
B、分子个数N=$\frac{m}{M}{N}_{A}$;
C、溶液体积不明确;
D、过氧化钠与二氧化碳的反应为歧化反应.
解答 解:A、标况下水为液态,故不能根据气体摩尔体积来计算其物质的量和分子个数,故A错误;
B、32g氧气中的分子个数N=$\frac{m}{M}{N}_{A}$=$\frac{32g}{32g/mol}{N}_{A}/mol$=NA个,28g氮气中的分子个数N=$\frac{28g}{28g/mol}{N}_{A}/mol$=NA个,故B正确;
C、溶液体积不明确,故溶液中的氯离子的个数无法计算,故C错误;
D、过氧化钠与二氧化碳的反应为歧化反应,1mol过氧化钠转移1mol电子即NA个,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


科目:高中化学 来源: 题型:解答题
 (一)发生在天津港“8•12”特大火灾爆炸事故,再一次引发了人们对环境问题的关注.
(一)发生在天津港“8•12”特大火灾爆炸事故,再一次引发了人们对环境问题的关注.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 燃放的焰火是某些金属元素焰色反应所呈现出来的色彩 | |
| B. | 小苏打是制作馒头和面包等糕点的膨松剂,还是治疗胃酸过多的一种药剂 | |
| C. | 为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅胶 | |
| D. | 可用漂白粉和漂白液对地震后的受灾地区进行杀菌消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上第一次月考化学卷(解析版) 题型:填空题
50mL0.50mol/L盐酸与50mL0.55mol/LNaO H溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
H溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
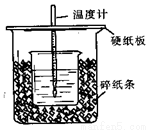
(1)从实验装置上看,图中尚缺少的一种玻璃用品是_______________。
(2)烧杯间填满碎纸条的作用是______________。
(3)大烧杯上如不盖硬纸板,求得的中和热数值____________(填“偏大”、“偏小”、“无影响”)。
(4)实验中60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量__________(填“相等”、“不相等”),所求中和热___________(填“相等”、“不相等”)。
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会_________(均填“偏大”、“偏小”、“无影响”);用50mL0.50mol/LNaOH溶液进行上述实验,测得的中和热的数值会__________(均填“偏大”、“偏小”、“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | 物质 | 杂质 | 除杂质所选用的试剂或操作方法 |
| A | Mg | Al | 加入过量盐酸溶液,充分反应,过滤 |
| B | NaHCO3溶液 | Na2CO3溶液 | 加入足量氢氧化钡溶液,充分反应,过滤 |
| C | NO | NO2 | 通过盛有水的洗气瓶,再干燥 |
| D | FeCl3溶液 | FeCl2溶液 | 加入过量的铁粉,充分反应,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,14gN2含有的分子数为0.5NA | |
| B. | 标准状况下,11.2LH2O含有的分子数为0.5NA | |
| C. | 0.1mol•L-1的NaOH溶液中含钠离子数为0.1NA | |
| D. | 1.8gNH4+中含有的电子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只需加KSCN溶液 | B. | 只需加NaOH溶液 | ||
| C. | 先加KSCN溶液,再加氯水 | D. | 先加氯水,再加KSCN溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com