
分析 (1)依据n=$\frac{V}{{V}_{m}}$=$\frac{m}{M}$计算;
(2)CO、CO2的摩尔质量分别是28g/mol、44g/mol,等质量的CO、CO2,根据n=$\frac{m}{M}$,知,相同质量的CO和二氧化碳,其物质的量之比等于摩尔质量反比=44g/mol:28g/mol=11:7,根据V=nVm知,相同条件下,其体积之比等于物质的量之比;
(3)利用m=n×M来计算质量及质量之比,分子数之比等于物质的量之比;
(4)过氧化钠与水反应生成NaOH和氧气.
解答 解:(1)在标准状况下,气体的体积为0.672L,物质的量为$\frac{0.672L}{22.4L/mol}$=0.03mol,则气体摩尔质量M=$\frac{1.32g}{0.03mol}$=44g/mol;
故答案为:44g/mol;
(2)CO、CO2的摩尔质量分别是28g/mol、44g/mol,其摩尔质量之比=28g/mol:44g/mol=7:11,等质量的CO、CO2,根据n=$\frac{m}{M}$知,相同质量的CO和二氧化碳,其物质的量之比等于摩尔质量反比=44g/mol:28g/mol=11:7,根据V=nVm知,相同条件下,其体积之比等于物质的量之比=11:7,故答案为:7:11; 11:7;
(3)氧气与臭氧的质量之比为6mol×32g/mol:4mol×48g/mol=1:1,
因分子数之比等于物质的量之比,则分子个数之比为0.6mol:0.4mol=3:2,
故答案为:1:1;3:2;
(4)过氧化钠与水反应生成NaOH和氧气,离子反应为2Na2O2+2H2O=4Na++4OH-+O2↑,故答案为:2Na2O2+2H2O=4Na++4OH-+O2.
点评 本题考查阿伏伽德罗定律及其推论,熟练掌握物质的量有关公式,明确物质的量公式中各个物理量的关系是解本题关键,题目难度不大.


 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 在放电时,两极质量均增加 | |
| B. | 在充电时,电池中硫酸的浓度不断变小 | |
| C. | 在放电时,负极发生的反应是 Pb+2e-+SO42-=PbSO4 | |
| D. | 在放电时,正极发生的反应是 PbSO4+2e-=Pb+SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 反应物 | 起始温度t1/℃ | 终了温度t2/℃ | 中和热/kJ•mol-1 |
| A.1.0mol/L HCl溶液50mL、1.1mol/L NaOH溶液50mL | 13.0 | △H1 | |
| B.1.0mol/L HCl溶液50mL、1.1mol/L NH3•H2O溶液50mL | 13.0 | △H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | X | Y | Z |
| 初始浓度(mol•L-1) | 0.1 | 0.2 | 0 |
| 平衡浓度(mol•L-1) | 0.05 | 0.05 | 0.1 |
| A. | 反应可表示为X+3Y?2Z,其平衡常数为1600 | |
| B. | 增大压强使平衡向生成Z的方向移动,平衡常数增大 | |
| C. | 反应达到平衡时,X的转化率为50% | |
| D. | 反应起始时和达平衡时的压强比为3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
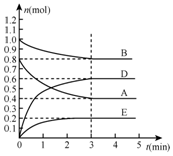 在某个容积为2L的密闭容器内,在T℃时按下图1所示发生反应:mA(g)+nB(g)?pC(g)+qE(s),△H<0(m、n、p、q为最简比例的整数).
在某个容积为2L的密闭容器内,在T℃时按下图1所示发生反应:mA(g)+nB(g)?pC(g)+qE(s),△H<0(m、n、p、q为最简比例的整数).查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | 上述反应的原子利用率可达到100% | |
| B. | 在核磁共振氢谱中对羟基扁桃酸应该有8个吸收峰 | |
| C. | 对羟基扁桃酸可以发生加成反应、取代反应和缩聚反应 | |
| D. | 1 mol对羟基扁桃酸与足量NaOH溶液反应,消耗3mol NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若X+和Y2-的核外电子层结构相同,则原子序数:X>Y | |
| B. | 卤族元素的最高正化合价等于其主族序数 | |
| C. | 元素周期表中从ⅢB族到ⅡB族十个纵列的元素都是金属元素 | |
| D. | Cs和Ba分别位于第六周期IA和IIA族,碱性:CsOH>Ba(OH)2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com