
| A. | 1mol CH2=CHCH3中含有σ键数为9NA | |
| B. | Na2O2与足量H2O反应,当生成0.1mol O2时,转移电子的数目为0.2NA | |
| C. | 1L 1.0mol/L CH3COONa溶液与2L 0.5mol/L CH3COONa溶液都含有NA个CH3COO- | |
| D. | 粗铜电解精炼纯铜,当电路中通过的电子数目为0.2NA时,阳极质量减少6.4g |
分析 A.1个CH2=CHCH3中含有6个C-H键,1个C-C键,共7个σ键;
B.Na2O2与H2O的反应是歧化反应,过氧化钠既是氧化剂又是还原剂;
C.醋酸根离子为弱酸根离子,存在水解;
D.电解精炼铜过程中,阳极粗铜中含有杂质铁、锌等,所以阳极质量减少6.4g时,转移的电子的物质的量不一定是0.2mol.
解答 解:A.1mol CH2=CHCH3中含有σ键数为7NA,故A错误;
B.Na2O2与H2O的反应是歧化反应:2Na2O2+2H2O=4NaOH+O2↑此反应转移2mol电子,生成1molO2,故当生成0.1molO2,转移电子0.2mol,数目为0.2NA,故B正确;
C.醋酸钠溶液中,醋酸根离子存在水解,所以1L 1.0mol/L CH3COONa溶液与2L 0.5mol/L CH3COONa溶液都含有小于NA个CH3COO-,故C错误;
D.粗铜中含有杂质铁、锌等,所以阳极减少6.4g时,电路中转移的电子的物质的量不一定为0.2mol,转移的电子数不一定为0.2NA,故D错误;
故选:B.
点评 本题考查阿伏加德罗常数的有关计算和判断,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,注意盐类的水解、电解法精炼铜的原理,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 结论 |
| A | 讲盛满氯气的试管倒扣在水槽中,放在日光下静置一段时间 | 气体逐渐减少,最后变为无色 | Cl2置换出水中的氧生成了O2 |
| B | 向某溶液中滴加氯水后,再加KSCN溶液 | 溶液呈红色 | 溶液中一定含有Fe2+ |
| C | 向饱和Na2CO3溶液中通入足量的CO2 | 溶液变浑浊 | 溶解度:NaHCO3<Na2CO3 |
| D | 向氯水中滴加紫色石蕊试剂 | 溶液变红 | 氯水显酸性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | K+ Ag+ Mg2+ Cu2+ Al3+ NH4+ |
| 阴离子 | Cl- CO32- NO3- SO42- SiO32- I- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | 除杂试剂 | 除杂方法 | |
| A | 乙烷(乙烯) | 氢气 | 加热 |
| B | 乙酸(乙醇) | 氢氧化钠溶液 | 蒸发 |
| C | 乙酸乙酯(乙酸) | 饱和碳酸钠溶液 | 分液 |
| D | 溴苯(苯) | 溴水 | 常温 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
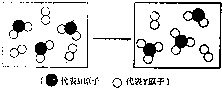 元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大.已知Y元素原子最外层电子数与核外电子总数之比为3:4,M元素原子的最外层电子数与次外层电子数之为3:4,且M原子的质子数是Y原子的2倍;N-、Z+、X+的半径逐渐减小;化合物XN在常温下为气体,据此回答下列问题:
元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大.已知Y元素原子最外层电子数与核外电子总数之比为3:4,M元素原子的最外层电子数与次外层电子数之为3:4,且M原子的质子数是Y原子的2倍;N-、Z+、X+的半径逐渐减小;化合物XN在常温下为气体,据此回答下列问题: .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.074 | 0.099 | 0.110 | 0.160 | 0.077 |
| 主要化合价 | -2 | +7、-1 | +5,-3 | +2 | +4、-4 |
 ;
;
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,由x g NO2和y g N2O4组成的混合气体中原子总数为3NA,则x+y=46 | |
| B. | 1mol氯气参加氧化还原反应,一定得到2NA个电子 | |
| C. | 1L 0.1mol•L-1NaBr溶液中,HBr和Br-总和为0.1NA个 | |
| D. | 12.5mL 16mol•L-1浓硫酸与足量铜反应,生成SO2的分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com