
【题目】下列可以大量共存的离子组是( )
A. 无色透明溶液中:NH4+、Cu2+、Cl﹣、NO3﹣
B. 碱性溶液中:K+、Na+、SO42﹣、Cl﹣
C. 酸性溶液中:K+、Na+、HCO3﹣、Ca2+
D. 酸性溶液中:Na+、Fe2+、SO42﹣、ClO﹣
 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】a、b、c、d、e、f分别是H、C、N、Na、Si、Cu六种元素中的其中一种,已知:图1表示的是六种元素单质的熔点高低顺序,其中c、d均是热和电的良导体,f形成的某种单质硬度最大。
回答下列问题:
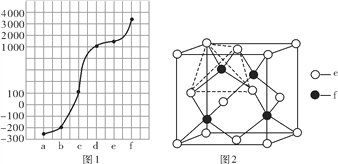
(1)a、b、f三种元素的电负性从小到大的顺序为________(用元素符号表示)。
(2)元素b的单质的一个分子中含有________个σ键和_________个π键。
(3)元素c的单质的晶体堆积方式类型是_______________________;若c单质分别与氟气和氯气形成化合物甲和乙,则甲的晶格能________乙的晶格能(填“>”“<”或“=”)。
(4)元素d的基态原子的价电子排布式为__________________。
(5)元素e和f可形成化合物丙(丙的晶胞结构如图2所示),则丙的化学式为_________;丙的晶体类型为_______________,在丙中,每个e原子周围最近的e原子数目为_____,若晶胞的边长为a pm,则丙的密度为____________g·cm-3(用NA表示阿伏加德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g)![]() 2SO3(g) △H<0,400℃时体积相同的甲、乙、丙三个容器中,甲容器绝热恒容,充入2molSO2和1molO2,乙容器恒温恒容,充入2molSO3,丙容器恒温恒压,充入2molSO3,充分反应达到平衡,下列说法正确的是
2SO3(g) △H<0,400℃时体积相同的甲、乙、丙三个容器中,甲容器绝热恒容,充入2molSO2和1molO2,乙容器恒温恒容,充入2molSO3,丙容器恒温恒压,充入2molSO3,充分反应达到平衡,下列说法正确的是
A. 甲和乙中反应的化学平衡常数相同
B. 乙和丙中的二氧化硫的生成速率相同
C. 乙中SO2的体积分数大于丙
D. 转化率:α甲(SO2)+α乙(SO3)<1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三硫化磷(P4S3)是黄绿色针状晶体,易燃、有毒,分子结构之一如下图所示,己知其燃烧热ΔH=-3677kJ/mol(P被氧化为P4O10),下列有关P4S3 的说法中不正确的是
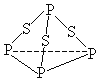
A. P4S3中磷元素为+3价
B. 分子中每个原子最外层均达到8电子稳定结构
C. 热化学方程式为P4S3(s)+8O2(g)=P4O10(s)+3SO2(g);△H=-3677kJ/mol
D. 分子中存在极性键与非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某金属与氯气反应生成的化合物中,其质量比为1∶1.9,原子个数比为1∶3,则金属的相对原子质量为
A. 27 B. 56 C. 23 D. 64
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A.【物质结构与性质】
甲基呋喃与氨在高温下反应得到甲基吡咯:

![]()
(1)Zn的基态原子核外电子排布式为______________。
(2)配合物[Zn(NH3)3(H2O)]2+中,与Zn2+形成配位键的原子是_____________(填元素符号)。
(3)1 mol甲基呋喃分子中含有σ键的数目为_______________mol。
(4)甲基吡咯分子中碳原子轨道的杂化轨道类型是____________。与NH3分子互为等电子体的阳离子为_____________。
(5)甲基吡咯的熔沸点高于甲基呋喃的原因是____________。
(6)锌的某种化合物晶胞结构如图所示,则构成该化合物的两种粒子个数比为____________
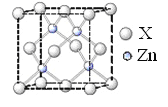
B.【实验化学】
硫酰氯(SO2Cl2)可用作有机化学的氯化剂,在药物和染料的制取中也有重要作用。某化学学习小组拟用干燥的Cl2和SO2在活性炭催化下制取硫酰氯。反应的化学方程式为:SO2(g)+ Cl2(g) =SO2Cl2(l) ΔH =97.3 kJ·mol1,实验装置如图所示(部分夹持装置未画出)。

已知:硫酰氯通常条件下为无色液体,熔点54.1℃,沸点69.1℃。在潮湿空气中“发烟”;100°C以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解。
回答下列问题:
(1)装置丙的冷凝管中冷凝水的入口是_____________(填“a”或“b”),装置己的作用是____________;如何控制两种反应物体积相等:______________。
(2)装置戊上方分液漏斗中最好选用下列试剂:_____________(选填字母)。
A.蒸馏水 B.饱和食盐水 C.浓氢氧化钠溶液 D.6.0 molL1盐酸
(3)若缺少装置乙和丁(均盛放浓硫酸),潮湿氯气和二氧化硫发生反应的化学方程式是_____________。
(4)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯:2ClSO3H![]() SO2Cl2 + H2SO4,分离两种产物的方法是____________(选填字母)。
SO2Cl2 + H2SO4,分离两种产物的方法是____________(选填字母)。
A.重结晶 B.过滤 C.蒸馏 D.萃取
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com