
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
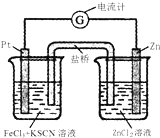 298K时,在FeCl3酸性溶液中加少量锌粒后,Fe3+ 立即被还原成Fe2+.据此某学习小组设计如图所示的原电池装置.下列有关说法正确的是( )
298K时,在FeCl3酸性溶液中加少量锌粒后,Fe3+ 立即被还原成Fe2+.据此某学习小组设计如图所示的原电池装置.下列有关说法正确的是( )| A、正极反应为Zn-2e-═Zn2+ |
| B、左烧杯中溶液的红色变浅 |
| C、Pt电极上有气泡出现 |
| D、该电池总反应为3Zn+2Fe3+═2Fe+3Zn2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、既不是氧化剂也不是还原剂 |
| B、是氧化剂 |
| C、既是氧化剂又是还原剂 |
| D、是还原剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com