
(1)相同物质的量浓度、相同体积的NaCl、MgCl2、AlCl3溶液,分别与足量的AgNO3溶液反应,生成沉淀的质量之比为________。
(2)向等体积、等浓度的AgNO3溶液中,分别加入相同体积的NaCl、MgCl2、AlCl3溶液,恰好使它们中的Cl-完全转化为AgCl沉淀,则三种溶液的物质的量浓度之比为________。
(3)Na、Mg、Al分别与足量的硫酸溶液反应,当生成气体的质量相同时,消耗Na、Mg、Al的物质的量之比为________。
(4)足量的Al分别与等浓度的硫酸、氢氧化钠溶液反应,当生成气体的质量相同时,硫酸溶液和氢氧化钠溶液的体积比为________。
【知识点】物质的量浓度 常见金属的性质A3 C1 C2
【答案解析】(1)1:2:3 (2)6:3:2 (3)6:3:2 (4)3:2
解析:(1)相同物质的量浓度、相同体积的NaCl、MgCl2、AlCl3溶液,氯离子的物质的量之比是1:2:3,分别与足量的AgNO3溶液反应,生成沉淀的质量之比为1:2:3。
(2)向等体积、等浓度的AgNO3溶液中,分别加入相同体积的NaCl、MgCl2、AlCl3溶液,恰好使它们中的Cl-完全转化为AgCl沉淀,就是求氯离子的物质的量浓度相等时三种溶液的物质的量浓度之比,即1:1/2:1/3=6:3:2。
(3)Na、Mg、Al分别与足量的硫酸溶液反应,当生成气体的质量相同时,问消耗Na、Mg、Al的物质的量之比,就是求转移等量电子时消耗Na、Mg、Al的物质的量之比,即1:1/2:1/3=6:3:2。
(4)反应分别为2Al+3H2SO4=Al2(SO4)3+3H2↑;2Al+2NaOH+2H2O=2NaAlO2+3H2↑当生成气体的质量相同时,硫酸溶液和氢氧化钠溶液的体积比为3:2。
【思路点拨】本题考查了物质的量浓度的理解以及金属的性质,理解氧化还原反应规律、顺利书写方程式是关键。


 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
我国城市环境污染中的大气污染物主要是 ( )。
A.CO2、Cl2、N2、酸雨
B.SO2、NO2、CO、烟尘
C.NH3、CO2、NO、雾
D.HCl、SO2、N2、粉尘
查看答案和解析>>
科目:高中化学 来源: 题型:
关于晶体的下列说法正确的是( )
A.在晶体中只要有阴离子就一定有阳离子
B.在晶体中只要有阳离子就一定有阴离子
C.原子晶体的熔点一定比金属晶体的高
D.分子晶体的熔点一定比金属晶体的低
查看答案和解析>>
科目:高中化学 来源: 题型:
0.4 mol CuCl2溶于水,配成1 L溶液,用石墨电极进行电解,当一个电极得到0.3 mol Cu时,另一个电极上生成的气体在标准状况下的体积是( )
A.5.6 L B.6.72 L
C.3.36 L D.11.2 L
查看答案和解析>>
科目:高中化学 来源: 题型:
“西气东输”是我国开发的重点工程,这里的气是指天然气,其主要成分是甲烷。工业上将碳与水在高温下反应制得水煤气,水煤气的主要成分是CO和H2,二者的体积比为11。已知1 mol CO气体完全燃烧生成CO2气体放出282.6 kJ热量;1 mol氢气完全燃烧生成液态水放出285.8 kJ热量;1 mol CH4气体完全燃烧生成CO2气体和液态水放出889.6 kJ热量。
(1)写出氢气完全燃烧生成液态水的热化学方程式:
________________________________________________________________________________________________________________________________________________。
(2)若1 mol CH4气体完全燃烧生成CO2气体和水蒸气,放出的热量________(填“大于”“等于”或“小于”)889.6 kJ。
(3)忽略水煤气中其他成分,相同状况下若得到相等的热量,所需水煤气与甲烷的体积比约为(整数比)________。
(4)以上数据和计算说明,以天然气替代水煤气作燃料,突出的优点是____________________________________________________ ____________________________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
ClO2在常温下是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。工业上用稍潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得。某学生拟用图1所示装置模拟工业制取并收集ClO2。
2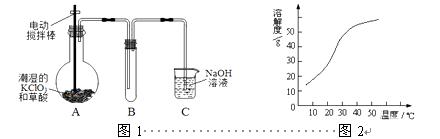
(1)A装置电动搅拌棒的作用是 。A装置必须添加温度控制装置,除酒精灯外,还需要的玻璃仪器有烧杯、 。
(2)B装置必须放在冰水浴中,其原因是 。
(3)反应后在装置C中可得NaClO2溶液。已知(1)NaClO2饱和溶液在温度低于38℃时析出晶体是NaClO2·3H2O,在温度高于38℃时析出晶体是NaClO2,温度高于60℃时NaClO2分解生成NaClO3和NaCl;(2)NaClO2的溶解度曲线如图2所示,请补充从NaClO2溶液中制得NaClO2晶体的操作步骤:
①减压,55℃蒸发结晶;② ;③ ;④低于60℃干燥;得到成品。
(4)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的含量,进行了下列实验:
步骤1:准确量取ClO2溶液10.00 mL,稀释成100.00 mL试样;量取V1 mL试样加入到锥形瓶中;
步骤2:用稀硫酸调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;
步骤3:加入指示剂,用c mol·L-1 Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2 mL(已知2 Na2S2O3 + I2 =Na2S4O6 + 2NaI)。
①配制100 mL c mol·L-1 Na2S2O3标准溶液时,用到的玻璃仪器除烧杯、量筒、玻璃棒外还有: 。
②滴定过程中进行三次平行测定的原因是 。
③若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果 。(填“偏高”、“偏低”或“不变” )
查看答案和解析>>
科目:高中化学 来源: 题型:
将0.5L 1mol/L FeCl3溶液加水稀释至1L,所得溶液中氯离子的物质的量浓度是()
A. 3mol/L B. 2mol/L C. 1.5mol/L D. 1mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
同温同体积同质量的CO2、CO、H2、O2的压强,按从大到小的顺序排列正确的是()
A. H2>O2>CO>CO2 B. H2>CO>O2>CO2 C. CO2>O2>CO>H2 D. CO2>H2>O2>CO
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com