
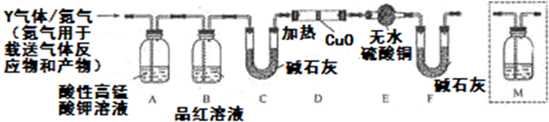
·ÖĪö £Ø1£©ŅĄ¾ŻÅØĮņĖįµÄĒæŃõ»ÆŠŌ½ā“š£»
£Ø2£©¢Ł¶ž¼ŪĢśĄė×Ó¾ßÓŠĒæµÄ»¹ŌŠŌ£¬Äܹ»Ź¹ĖįŠŌµÄøßĆĢĖį¼ŲĶŹÉ«£¬¼ģŃéFe2+£¬æÉĄūÓĆ+2¼ŪŃĒĢśĄė×ÓÄÜŹ¹Ėį»ÆµÄøßĆĢĖį¼ŲĶŹÉ«Ą“¼ģŃ飻
¢ŚÉś³ÉµÄSO2¾ßÓŠ»¹ŌŠŌ£¬ĶØČė×ćĮæäåĖ®ÖŠ£¬·¢ÉśSO2+Br2+2H2O=2HBr+H2SO4£¬ĄūÓĆĮņŌŖĖŲµÄŹŲŗć£¬½įŗĻ¹ŲĻµŹ½£ŗSO2”śBaSO4Ēó³öSO2µÄĢå»ż·ÖŹż£»
£Ø3£©¶žŃõ»ÆĮņÄÜŹ¹Ę·ŗģČÜŅŗĶŹÉ«£¬“Ó¶ų¼ģŃ鶞Ńõ»ÆĮņŹĒ·ń³ż¾”£»
£Ø4£©¼ÓČČĢõ¼žĻĀ£¬CŗĶÅØĮņĖį·“Ӧɜ³É¶žŃõ»ÆĢ¼£»
£Ø5£©ŌŚČ·¶Ø²»“ęŌŚ¶žŃõ»ÆĮņĢõ¼žĻĀ£¬½«ĘųĢåĶØČė³ĪĒåŹÆ»ŅĖ®¼ģŃéŹĒ·ńŗ¬ÓŠ¶žŃõ»ÆĢ¼£»
£Ø6£©ĒāĘų¾ßÓŠ»¹ŌŠŌ£¬ÄÜ»¹ŌŠŌ£¬ÄÜ»¹ŌŗŚÉ«µÄŃõ»ÆĶÉś³ÉŗģÉ«µÄĶµ„ÖŹ£¬Ķ¬Ź±Éś³ÉĖ®£¬Ė®ÄÜŹ¹ĪŽĖ®ĮņĖįĶ±äĄ¶É«£®
½ā“š ½ā£ŗ£Ø1£©ÅØĮņĖį¾ßÓŠĒæµÄŃõ»ÆŠŌ£¬³£ĪĀĻĀÓöµ½Ģś·¢Éś¶Ū»Æ£¬ŠĪ³ÉÖĀĆÜŃõ»ÆĤ×čÖ¹·“Ó¦½ųŠŠ£»
¹Ź“š°øĪŖ£ŗ³£ĪĀĻĀÅØĮņĖįŹ¹Ģś¶Ū»Æ£»
£Ø2£©¢Ła£®ČÜŅŗÖŠŗ¬ÓŠČż¼ŪĢśĄė×Ó£¬Óöµ½ĮņĒčĖį¼ŲĻŌŗģÉ«£¬¶Ō¶ž¼ŪĢśĄė×Ó¼ģŃéŌģ³ÉøÉČÅ£¬¹Źa²»Ń”£»
b£®ČÜŅŗÖŠŗ¬ÓŠČż¼ŪĢśĄė×Ó£¬ŗĶNaOH·“Ӧɜ³ÉŗģŗÖÉ«³Įµķ£¬ŃĒĢśĄė×ÓŗĶNaOH·“Ӧɜ³É°×É«³Įµķ£¬µ«²»ĪČ¶Ø£¬Į¢¼“×Ŗ»ÆĪŖ»ĘĀĢÉ«×īÖÕ×Ŗ»ÆĪŖŗģŗÖÉ«³Įµķ£¬ĖłŅŌĪŽĀŪŹĒ·ńŗ¬ÓŠŃĒĢśĄė×Ó£¬¼ÓČėÅØ°±Ė®¶¼²śÉśŗģŗÖÉ«³Įµķ£¬¹Źb²»Ń”£»
c£®ŃĒĢśĄė×ÓŗĶÅØ°±Ė®·“Ӧɜ³É°×É«³Įµķ£¬µ«²»ĪČ¶Ø£¬Į¢¼“×Ŗ»ÆĪŖ»ĘĀĢÉ«×īÖÕ×Ŗ»ÆĪŖŗģŗÖÉ«³Įµķ£¬ĢśĄė×ÓŗĶÅØ°±Ė®·“Ӧɜ³ÉŗģŗÖÉ«³Įµķ£¬ĖłŅŌĪŽĀŪŹĒ·ńŗ¬ÓŠŃĒĢśĄė×Ó£¬¼ÓČėÅØ°±Ė®¶¼²śÉśŗģŗÖÉ«³Įµķ£¬¹Źc²»Ń”£»
d£®¶ž¼ŪĢśĄė×Ó¾ßÓŠĒæµÄ»¹ŌŠŌ£¬Äܹ»Ź¹ĖįŠŌµÄøßĆĢĖį¼ŲĶŹÉ«£¬Čż¼ŪĢśĄė×Ó²»¾ßÓŠ»¹ŌŠŌ£¬²»ÄÜŹ¹øßĆĢĖį¼ŲĶŹÉ«£¬ĖłŅŌæÉŅŌÓĆĄ“¼ģŃ鶞¼ŪĢśĄė×Ó£¬¹ŹdŃ”£»
¹ŹŃ”£ŗd£»
¢ŚSO2¾ßÓŠ»¹ŌŠŌ£¬ĶØČė×ćĮæäåĖ®ÖŠ£¬·¢ÉśSO2+Br2+2H2O=2HBr+H2SO4£¬
n£Ø»ģŗĻĘųĢ壩=$\frac{0.336L}{22.4L/mol}$=0.015mol£¬
SO2 ”śBaSO4
1mol 233g
n 2.33g
n=0.01mol£»
Ōņ SO2µÄĢå»ż·ÖŹż£ŗ$\frac{0.01mol}{0.015mol}$”Į100%=66.7%£¬
¹Ź“š°øĪŖ£ŗ66.7%£»
£Ø3£©A³żČ„¶žŃõ»ÆĮņ£¬¶žŃõ»ÆĮņÄÜŹ¹Ę·ŗģČÜŅŗĶŹÉ«£¬ĖłŅŌBæÉŅŌ¼ģŃéAÖŠŹĒ·ńĶźČ«³żČ„¶žŃõ»ÆĮņ£¬
¹Ź“š°øĪŖ£ŗ¼ģŃéSO2ŹĒ·ń³ż¾”£»
£Ø4£©¼ÓČČĢõ¼žĻĀ£¬CŗĶÅØĮņĖį·“Ӧɜ³É¶žŃõ»ÆĢ¼£¬ĖłŅŌQŹĒ¶žŃõ»ÆĢ¼£¬·“Ó¦·½³ĢŹ½ĪŖC+2H2SO4£ØÅØ£©$\frac{\underline{\;\;”÷\;\;}}{\;}$2SO2”ü+CO2”ü+2H2O£¬
¹Ź“š°øĪŖ£ŗC+2H2SO4£ØÅØ£©$\frac{\underline{\;\;”÷\;\;}}{\;}$2SO2”ü+CO2”ü+2H2O£»
£Ø5£©ŹµŃéŹŅÓĆ³ĪĒåŹÆ»ŅĖ®¼ģŃ鶞Ńõ»ÆĢ¼£¬µ«¶žŃõ»ÆĮņŅ²ÄÜŹ¹³ĪĒåŹÆ»ŅĖ®±ä»ė×Ē£¬ŅŖ¼ģŃ鶞Ńõ»ÆĢ¼Ó¦øĆÅųż¶žŃõ»ÆĮņµÄøÉČÅ£¬ĖłŅŌŌŚČ·¶Ø²»“ęŌŚ¶žŃõ»ÆĮņĢõ¼žĻĀ£¬½«ĘųĢåĶØČė³ĪĒåŹÆ»ŅĖ®¼ģŃéŹĒ·ńŗ¬ÓŠ¶žŃõ»ÆĢ¼£¬øĆ¼ģŃé×°ÖĆÓ¦øĆŌŚB-CÖ®¼ä£¬
¹ŹŃ”c£¬
¹Ź“š°øĪŖ£ŗc£»
£Ø6£©ĒāĘų¾ßÓŠ»¹ŌŠŌ£¬ÄÜ»¹ŌŠŌ£¬ÄÜ»¹ŌŗŚÉ«µÄŃõ»ÆĶÉś³ÉŗģÉ«µÄĶµ„ÖŹ£¬Ķ¬Ź±Éś³ÉĖ®£¬Ė®ÄÜŹ¹ĪŽĖ®ĮņĖįĶ±äĄ¶É«£¬ÕāŹĒ¼ģŃéĖ®µÄĢŲÕ÷·“Ó¦£¬ĖłŅŌČē¹ūDÖŠŃõ»ÆĶ±äŗģ£¬EÖŠĪŽĖ®ĮņĖįĶ±äĄ¶£¬ŌņÖ¤Ć÷ŗ¬ÓŠĒāĘų£¬
¹Ź“š°øĪŖ£ŗDÖŠŗŚÉ«·ŪÄ©±äŗģ£¬EÖŠ°×É«·ŪÄ©±äĄ¶£®
µćĘĄ ±¾Ģā×ŪŗĻæ¼²éŌŖĖŲ»ÆŗĻĪļÖŖŹ¶£¬æ¼²éŠŌÖŹŹµŃé·½°øÉč¼Ę£¬ŹģĻ¤Ļą¹ŲĪļÖŹµÄŠŌÖŹŹĒ½āĢā¹Ų¼ü£¬×¢Ņā¶ž¼ŪĢśĄė×Ó”¢Čż¼ŪĢśĄė×ӵļģŃé·½·Ø£¬ĢāÄæÄѶČÖŠµČ£®


 Ó¦ÓĆĢā×÷Ņµ±¾ĻµĮŠ“š°ø
Ó¦ÓĆĢā×÷Ņµ±¾ĻµĮŠ“š°ø Źī¼Ł×÷ŅµŹī¼ŁæģĄÖĮ·Ī÷°²³ö°ęÉēĻµĮŠ“š°ø
Źī¼Ł×÷ŅµŹī¼ŁæģĄÖĮ·Ī÷°²³ö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĘĻĢŃĢĒÅضČĢ«“ó | B£® | ¼ÓČČŹ±¼ä²»¹» | ||
| C£® | CuSO4ČÜŅŗµÄĮæ²»¹» | D£® | NaOHČÜŅŗµÄĮæ²»¹» |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
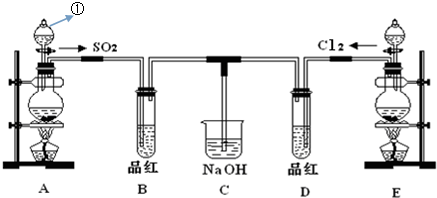
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
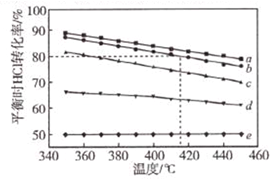 ĪÄĻױصĄ£ŗĄūÓĆĀČ»ÆĒāŃõ»Æ·“Ó¦Ņ»ĶŃĖ®ńīŗĻ¹¤ŅÕ£¬æÉÓĆÓŠ»śĀČ»Æ¹¤ŅÕµÄø±²śĘ·ĀČ»ÆĒāĪŖŌĮĻÖʱøĀČĘų£¬ŹµĻÖĀȵÄŃ»·ĄūÓĆ£¬ŌĄķĪŖ4HCl£Øg£©+O2£Øg£©?2Cl2£Øg£©+2H2O£Øg£©£®½«HC1ŗĶO2·Ö±šŅŌ5ÖÖĪļÖŹµÄĮæ±Č£ŗ¢Ł1£ŗ1 ¢Ś2£ŗ1 ¢Ū4£ŗ1 ¢Ü6£ŗ1 ¢Ż8£ŗ1£¬ĻņĪåøöČŻ»żæɱäµÄČŻĘ÷ÖŠĶ¶ĮĻŹ±£¬·“Ó¦ĪĀ¶Č¶ŌHClĘ½ŗā×Ŗ»ÆĀČÓ°ĻģµÄĒśĻßČēĶ¼£®
ĪÄĻױصĄ£ŗĄūÓĆĀČ»ÆĒāŃõ»Æ·“Ó¦Ņ»ĶŃĖ®ńīŗĻ¹¤ŅÕ£¬æÉÓĆÓŠ»śĀČ»Æ¹¤ŅÕµÄø±²śĘ·ĀČ»ÆĒāĪŖŌĮĻÖʱøĀČĘų£¬ŹµĻÖĀȵÄŃ»·ĄūÓĆ£¬ŌĄķĪŖ4HCl£Øg£©+O2£Øg£©?2Cl2£Øg£©+2H2O£Øg£©£®½«HC1ŗĶO2·Ö±šŅŌ5ÖÖĪļÖŹµÄĮæ±Č£ŗ¢Ł1£ŗ1 ¢Ś2£ŗ1 ¢Ū4£ŗ1 ¢Ü6£ŗ1 ¢Ż8£ŗ1£¬ĻņĪåøöČŻ»żæɱäµÄČŻĘ÷ÖŠĶ¶ĮĻŹ±£¬·“Ó¦ĪĀ¶Č¶ŌHClĘ½ŗā×Ŗ»ÆĀČÓ°ĻģµÄĒśĻßČēĶ¼£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 0.1 nm×óÓŅ | B£® | 50 nm×óÓŅ | C£® | 0.001 mm×óÓŅ | D£® | 100 mm×óÓŅ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆpHŹŌÖ½²āŹŌ | B£® | ÓĆĪÅĘųĪ¶ŗĶpHŹŌÖ½²āŹŌ | ||
| C£® | ÓĆBa£ØOH£©2ČÜŅŗŗĶ·ÓĢŖŹŌŅŗ | D£® | ÓĆNaOHŗĶBaCl2ČÜŅŗ¼ų±š |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
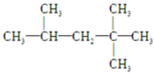 £¬ĖüŹĒĘūÓĶČ¼ÉÕĘ·ÖŹæ¹ÕšŠŌÄܵIJĪÕÕĪļ£¬ĘäÖŠAµÄĶ¬·ÖŅģ¹¹ĢåÖŠŗ¬µČŠ§ĒāŌ×ÓÖÖĄą×īÉŁµÄŅ»ÖÖ½į¹¹¼ņŹ½ĪŖ£ŗ
£¬ĖüŹĒĘūÓĶČ¼ÉÕĘ·ÖŹæ¹ÕšŠŌÄܵIJĪÕÕĪļ£¬ĘäÖŠAµÄĶ¬·ÖŅģ¹¹ĢåÖŠŗ¬µČŠ§ĒāŌ×ÓÖÖĄą×īÉŁµÄŅ»ÖÖ½į¹¹¼ņŹ½ĪŖ£ŗ £»ČōAŹĒÓÉĻ©ĢžŗĶH2Ķعż¼Ó³É·“Ó¦µĆµ½£¬ŌņøĆĻ©ĢžµÄ½į¹¹¼ņŹ½ĪŖ
£»ČōAŹĒÓÉĻ©ĢžŗĶH2Ķعż¼Ó³É·“Ó¦µĆµ½£¬ŌņøĆĻ©ĢžµÄ½į¹¹¼ņŹ½ĪŖ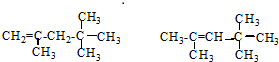 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | øŗ¼«·“Ó¦ĪŖ£ŗCu-2e-ØTCu2+ | |
| B£® | ČōøĆŌµē³Ų¹¤×÷Ē°Į½µē¼«ÖŹĮæĻąµČ£¬Ōņ¹¤×÷ŗ󣬵±ĶµÄÖŹĮæ¼õÉŁ6.4gŹ±£¬Į½µē¼«ÖŹĮæĻą²ī21.6g£Ø¼ŁÉčµē½āÖŹČÜŅŗ¶¼ŹĒ×ćĮæµÄ£© | |
| C£® | µ±ĶµÄÖŹĮæ¼õŠ”12.8 gŹ±£¬ĶāµēĀ·ÖŠĶعż0.4molµē×Ó | |
| D£® | Ōµē³ŲµÄ×Ü·“Ó¦Ź½ĪŖ£ŗCu+2AgNO3ØT2Ag+Cu£ØNO3£©2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com