
| 氢氧化钠质量(g) | 氯化钠质量(g) | |
| ① | 2.40 | 3.51 |
| ② | 2.32 | 2.34 |
| ③ | 3.48 | 3.51 |
| m |
| M |
| m |
| n |
| 3.51g |
| 58.5g/mol |
| 2.4g |
| 0.06mol |
| 2.34g |
| 58.5g/mol |
| 2.32g |
| 0.04mol |
| 58-40 |
| 18 |
| 3.51g |
| 58.5g/mol |
| 3.48g |
| 0.06mol |
| 58-40 |
| 18 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
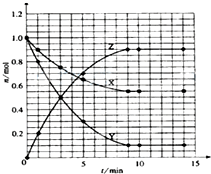 I、已知:2SO2(g)+O2(g)?2SO3(g)△H=-196.0kJ?mol-1
I、已知:2SO2(g)+O2(g)?2SO3(g)△H=-196.0kJ?mol-1查看答案和解析>>
科目:高中化学 来源: 题型:
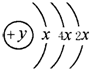 A、B、C、D四种短周期元素,原子序数D>A>B>C,且A、B同周期,C、D同主族,A的原子结构示意图如图,B元素最外层电子数是次外层电子数的四分之一,C元素的气态氢化物的水溶液显碱性,据此填空:
A、B、C、D四种短周期元素,原子序数D>A>B>C,且A、B同周期,C、D同主族,A的原子结构示意图如图,B元素最外层电子数是次外层电子数的四分之一,C元素的气态氢化物的水溶液显碱性,据此填空:查看答案和解析>>
科目:高中化学 来源: 题型:
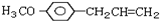 )医学上又叫升白宁,对肿瘤患者化疗和放疗所致的白细胞减少症有较好的疗效.根据题意完成下列填空:
)医学上又叫升白宁,对肿瘤患者化疗和放疗所致的白细胞减少症有较好的疗效.根据题意完成下列填空: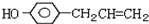 )与甲醇合成升白宁,该反应属于
)与甲醇合成升白宁,该反应属于查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 代号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 半径(pm) | 30 | 64 | 66 | 91 | 70 | 106 | 110 | 186 | 125 | 232 |
| 主要化合价 | -1,+1 | -1 | -2 | -4,+4 | -3,+5 | -2,+4,+6 | -4,+4 | +1 | +3 | +1 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、盐酸、天然气、醋酸、干冰 |
| B、胆矾、漂白粉、氯化钾、氯气 |
| C、氯化钠、汽油、硫酸钡、乙醇 |
| D、氢氧化钠、空气、苛性钾、石灰石 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com