
£Ø15·Ö£©ŌŚĶµÄ“ß»Æ×÷ÓĆĻĀ°±ŗĶ·ś·“Ó¦µĆµ½Ņ»ÖÖļ§ŃĪŗĶŅ»ÖÖČż½Ē׶Ģå·Ö×ÓA£Ø¼ü½Ē102o£¬Å¼¼«¾Ų0.78x10-30 C?m£»¶Ō±Č£ŗ°±µÄ¼ü½Ē107.3o£¬Å¼¼«¾Ų4.74x10-30 C?m)£»
4-1 Š“³öAµÄ·Ö×ÓŹ½ŗĶĖüµÄŗĻ³É·“Ó¦µÄ»Æѧ·½³ĢŹ½”£
4-2 A·Ö×ÓÖŹ×ӻƷųöµÄČČĆ÷ĻŌŠ”ÓŚ°±·Ö×ÓÖŹ×ӻƷųöµÄČČ”£ĪŖŹ²Ć“£æ
4-3 AÓė¹Æ¹²ČČ£¬µĆµ½Ņ»ÖÖ¹ÆŃĪŗĶŅ»¶Ō»„ĪŖŅģ¹¹ĢåµÄBŗĶC£ØĻą¶Ō·Ö×ÓÖŹĮæ66£©”£Š“³ö»Æѧ·½³ĢŹ½¼°BŗĶCµÄĮ¢Ģå½į¹¹”£4-4 BÓėĖÄ·ś»ÆĪż·“Ó¦Ź×ĻȵƵ½Ę½Ćę¹¹ŠĶµÄDŗĶøŗ¶ž¼Ūµ„ÖŠŠÄŅõĄė×ÓE¹¹³ÉµÄĄė×Ó»ÆŗĻĪļ£»ÕāÖÖĄė×Ó»ÆŗĻĪļŹÜČČ·Å³öC£¬Ķ¬Ź±µĆµ½DŗĶøŗŅ»¼Ūµ„ÖŠŠÄŅõĄė×ÓF¹¹³ÉµÄĄė×Ó»ÆŗĻĪļ”£»³öD”¢E”¢FµÄĮ¢Ģå½į¹¹£»Š“³öµĆµ½ĖüĆĒµÄ»Æѧ·½³ĢŹ½”£
4-5 AÓėF2”¢BF3·“Ó¦µĆµ½Ņ»ÖÖĖÄ·śÅšĖįŃĪ£¬ĖüµÄŃōĄė×ÓĖ®½āÄܶØĮæµŲÉś³ÉAŗĶHF£¬¶ųĶ¬Ź±µĆµ½µÄO2ŗĶH2O2µÄĮæČ“Ņņ·“Ó¦Ģõ¼ž²»Ķ¬¶ų²»Ķ¬”£Š“³öÕāøöŃōĄė×ӵĻÆѧŹ½ŗĶĖüµÄŗĻ³É·“Ó¦µÄ»Æѧ·½³ĢŹ½£¬²¢ÓĆ»Æѧ·½³ĢŹ½ŗĶ±ŲŅŖµÄĶʶĻ¶ŌĖüµÄĖ®½ā·“Ó¦²śĪļ×÷³ö½āŹĶ”£4-1 NF3 £Ø1·Ö£© 4NH3 + 3F2 = NF3 + 3NH4F£Ø1·Ö£© £Ø¹²2·Ö£©
4-2 N-F ¼üµÄż¼«·½ĻņÓėµŖŌ×Ó¹Ā¶Ōµē×ӵĿ¼«·½ĻņĻą·“£¬µ¼ÖĀ·Ö×Óż¼«¾ŲŗÜŠ”£¬Ņņ“ĖÖŹ×Ó»ÆÄÜĮ¦Ō¶±Č°±ÖŹ×Ó»ÆÄÜĮ¦Š””£ »Ķ¼ĖµĆ÷Ņ²æÉ£¬Čē£ŗ
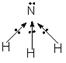
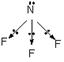 £Ø1·Ö£©
£Ø1·Ö£©
4-3 2NF3 +2Hg = N2F2 + 2HgF2 £Ø1·Ö£©
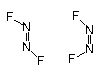 (14+19)X2=66 £ØĆæŹ½1·Ö£© £Ø¹²3·Ö£©
(14+19)X2=66 £ØĆæŹ½1·Ö£© £Ø¹²3·Ö£©
4-4£ŗ 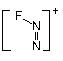 D
D  E
E 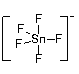 F £ØĆæŹ½1·Ö£©
F £ØĆæŹ½1·Ö£©
2 N2F2 + SnF4 = [N2F+]2[SnF6]2- £Ø1·Ö£©
[N2F+]2[SnF6]2- = [N2F] +[SnF5]- + N2F2 £Ø1·Ö£© £Ø¹²5·Ö£©
4-5 ŃōĄė×ӵĻÆѧŹ½ĪŖNF4+”££Ø1·Ö£©
NF3 + F2 + BF3 = NF4+BF4- £Ø1·Ö£©
NF4+Ė®½ā·“Ó¦Ź×ĻȵƵ½HOF £Ø·ńŌņŠ“²»³öÅäĘ½µÄNF4+Ė®½ā·“Ó¦£©:
NF4++H2O = NF3+HOF+H+ ¶ØĮæÉś³ÉNF3”££Ø1·Ö£©
¶ų·“Ó¦2HOF = 2HF+O2ŗĶ·“Ó¦HOF+H2O = HF+H2O2 ÄÄŅ»·“Ó¦ĪŖÖ÷Óė·“Ó¦Ģõ¼žÓŠ¹Ų£¬µ«ĪŽĀŪÄÄŅ»·“Ó¦ĪŖÖ÷Č“×ÜŹĒ¶ØĮæÉś³ÉHF”££Ø1·Ö£© £Ø¹²4·Ö£©



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
 £Ø2012?ÄĻ¾©Ä£Äā£©Čż·ś»ÆµŖ£ØNF3£©ŹĒŅ»ÖÖĪŽÉ«”¢ĪŽĪ¶”¢ĪŽ¶¾ĒŅ²»æÉČ¼µÄĘųĢ壬ŌŚ°ėµ¼Ģå¼Ó¹¤”¢Ģ«ŃōÄܵē³ŲÖĘŌģŗĶŅŗ¾§ĻŌŹ¾Ę÷ÖĘŌģÖŠµĆµ½¹ć·ŗÓ¦ÓĆ£®ĖüæÉŌŚĶµÄ“ß»Æ×÷ÓĆĻĀÓÉF2ŗĶ¹żĮæµÄNH3·“Ó¦µĆµ½£®
£Ø2012?ÄĻ¾©Ä£Äā£©Čż·ś»ÆµŖ£ØNF3£©ŹĒŅ»ÖÖĪŽÉ«”¢ĪŽĪ¶”¢ĪŽ¶¾ĒŅ²»æÉČ¼µÄĘųĢ壬ŌŚ°ėµ¼Ģå¼Ó¹¤”¢Ģ«ŃōÄܵē³ŲÖĘŌģŗĶŅŗ¾§ĻŌŹ¾Ę÷ÖĘŌģÖŠµĆµ½¹ć·ŗÓ¦ÓĆ£®ĖüæÉŌŚĶµÄ“ß»Æ×÷ÓĆĻĀÓÉF2ŗĶ¹żĮæµÄNH3·“Ó¦µĆµ½£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2011-2012ѧğ½ĖÕŹ”ÄĻĶØŹŠøßČżÉĻŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ ĢāŠĶ£ŗĢīæÕĢā
(16·Ö)Čż·ś»ÆµŖ£ØNF3£©ŹĒŅ»ÖÖĪŽÉ«”¢ĪŽĪ¶”¢ĪŽ¶¾ĒŅ²»æÉČ¼µÄĘųĢ壬ŌŚ°ėµ¼Ģå¼Ó¹¤”¢Ģ«ŃōÄܵē³ŲÖĘŌģŗĶŅŗ¾§ĻŌŹ¾Ę÷ÖĘŌģÖŠµĆµ½¹ć·ŗÓ¦ÓĆ”£ĖüæÉŌŚĶµÄ“ß»Æ×÷ÓĆĻĀÓÉF2ŗĶ¹żĮæµÄNH3·“Ó¦µĆµ½£¬øĆ·“Ó¦ĮķŅ»ÖÖ²śĪļĪŖŃĪ”£
£Ø1£©øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ ”ų £¬ĆæÉś³É1molNF3,×ŖŅʵĵē×ÓŹżĪŖ ”ų £¬Éś³ÉĪļNF3ÖŠµŖŌ×ÓµÄŌӻƷ½Ź½ĪŖ ”ų £¬NF3·Ö×Óæռ乹ŠĶĪŖ ”ų £»
£Ø2£©N”¢FĮ½ÖÖŌŖĖŲµÄĒā»ÆĪļĪČ¶ØŠŌ±Č½Ļ£¬NH3 ”ų HF£ØŃ”Ģī”°>”±»ņ”°<”±£©£»
£Ø3£©N3-±»³ĘĪŖĄąĀ±Ąė×Ó£¬Š“³ö1ÖÖÓėN3-»„ĪŖµČµē×ÓĢåµÄ·Ö×ӵĻÆѧŹ½ ”ų £»
£Ø4£© ĀČ»ÆĶČÜŅŗÖŠ¼ÓČė¹żĮæ°±Ė®£¬æÉŅŌÉś³ÉĖÄ°±ŗĻĶĀēĄė×Ó£¬ Š“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ ”ų £»
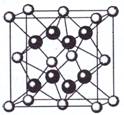
£Ø5£©ŌŖĖŲA»łĢ¬Ō×ÓµÄŗĖĶāµē×ÓÅŲ¼Ź½ĪŖ1s22s22p63s23p64s2£¬Aøś·śæÉŠĪ³ÉĄė×Ó»ÆŗĻĪļ£¬Ę侧°ū½į¹¹Čē×óĶ¼£¬øĆĄė×Ó»ÆŗĻĪļµÄ»ÆѧŹ½ĪŖ ”ų ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2011-2012Ń§ÄźÉ½Ī÷Ź”øßČż10ŌĀ·ŻŌĀæ¼»ÆѧŹŌ¾ķ ĢāŠĶ£ŗĢīæÕĢā
(16·Ö)Čż·ś»ÆµŖ£ØNF3£©ŹĒŅ»ÖÖĪŽÉ«”¢ĪŽĪ¶”¢ĪŽ¶¾ĒŅ²»æÉČ¼µÄĘųĢ壬ŌŚ°ėµ¼Ģå¼Ó¹¤”¢Ģ«ŃōÄܵē³ŲÖĘŌģŗĶŅŗ¾§ĻŌŹ¾Ę÷ÖĘŌģÖŠµĆµ½¹ć·ŗÓ¦ÓĆ”£ĖüæÉŌŚĶµÄ“ß»Æ×÷ÓĆĻĀÓÉF2ŗĶ¹żĮæµÄNH3·“Ó¦µĆµ½£¬øĆ·“Ó¦ĮķŅ»ÖÖ²śĪļĪŖŃĪ”£
£Ø1£©øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ £¬ĆæÉś³É1molNF3,×ŖŅʵĵē×ÓŹżĪŖ
Éś³ÉĪļNF3ÖŠµŖŌ×ÓµÄŌӻƷ½Ź½ĪŖ £¬NF3·Ö×Óæռ乹ŠĶĪŖ £»
£Ø2£©N”¢FĮ½ÖÖŌŖĖŲµÄĒā»ÆĪļĪČ¶ØŠŌ±Č½Ļ£¬NH3 HF£ØŃ”Ģī”°>”±»ņ”°<”±£©£»
£Ø3£©N3-±»³ĘĪŖĄąĀ±Ąė×Ó£¬Š“³ö1ÖÖÓėN3-»„ĪŖµČµē×ÓĢåµÄ·Ö×ӵĻÆѧŹ½ £»
£Ø4£©ĀČ»ÆĶČÜŅŗÖŠ¼ÓČė¹żĮæ°±Ė®£¬æÉŅŌÉś³ÉĖÄ°±ŗĻĶĀēĄė×Ó£¬ Š“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ £»
£Ø5£©ŌŖĖŲA»łĢ¬Ō×ÓµÄŗĖĶāµē×ÓÅŲ¼Ź½ĪŖ1s22s22p63s23p64s2£¬Aøś·śæÉŠĪ³ÉĄė×Ó»ÆŗĻĪļ£¬Ę侧°ū½į¹¹Čē×óĶ¼£¬øĆĄė×Ó»ÆŗĻĪļµÄ»ÆѧŹ½ĪŖ ”£

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
£Ø1£©ŗĻ³É°±¹¤Ņµ¶Ō»Æѧ¹¤ŅµŗĶ¹ś·Ą¹¤Ņµ¾ßÓŠÖŲŅŖŅāŅ唣¹¤ŅµŗĻ³É°±Éś²śŹ¾ŅāĶ¼ČēÓŅĶ¼ĖłŹ¾”£
¢ŁŗĻ³É°±Ģõ¼žŃ”¶ØµÄÖ÷ŅŖŌŅņŹĒ£ØŃ”Ģī×ÖÄøŠņŗÅ£© £»
A£®ĪĀ¶Č”¢Ń¹Ēæ¶Ō»Æѧ·“Ó¦ĖŁĀŹ¼°»ÆŃ§Ę½ŗāÓ°Ļģ
B£®Ģś“„Ć½ŌŚøĆĪĀ¶ČŹ±»īŠŌ“ó
C£®¹¤ŅµÉś²śŹÜ¶ÆĮ¦”¢²ÄĮĻ”¢Éč±øµČĢõ¼žµÄĻŽÖĘ
¢Śøı䷓ӦĢõ¼ž£¬Ę½ŗā»į·¢ÉśŅĘ¶Æ”£Ń¹ĒæŌö“ó£¬Ę½ŗā³£ŹżK (Ģī”°Ōö“ó”±”°¼õŠ””±”°²»±ä”±)
£Ø2£©°±Ęų¾ßÓŠ»¹ŌŠŌ£¬ŌŚĶµÄ“ß»Æ×÷ÓĆĻĀ£¬°±ĘųŗĶ·śĘų·“Ӧɜ³ÉAŗĶBĮ½ÖÖĪļÖŹ”£AĪŖļ§ŃĪ£¬BŌŚ±ź×¼×“æöĻĀĪŖĘųĢ¬”£ŌŚ“Ė·“Ó¦ÖŠ£¬ČōĆæ·“Ó¦1Ģå»ż°±Ęų£¬Ķ¬Ź±·“Ó¦0.75Ģå»ż·śĘų£»ČōĆæ·“Ó¦8.96L°±Ęų£Ø±ź×¼×“æö£©£¬Ķ¬Ź±Éś³É0.3molA”£
¢ŁŠ“³ö°±ĘųŗĶ·śĘų·“Ó¦µÄ»Æѧ·½³ĢŹ½ £»
¢ŚŌŚ±ź×¼×“æöĻĀ£¬ĆæÉś³É1 mol B£¬×ŖŅʵē×ӵďżÄæĪŖ ”£
(3) ×ī½üĆĄ¹śSimonsµČæĘѧ¼Ņ·¢Ć÷ĮĖ²»±ŲŹ¹°±ĻČĮŃ»ÆĪŖĒā¾ĶæÉÖ±½ÓÓĆÓŚČ¼ĮĻµē³ŲµÄ·½·Ø”£Ėü¼ČÓŠŅŗĒāČ¼ĮĻµē³ŲµÄÓÅµć£¬ÓÖæĖ·žĮĖŅŗĒā²»Ņ×±£“ęµÄ²»×ć”£Ęä×°ÖĆĪŖÓĆ²¬ŗŚ×÷ĪŖµē¼«£¬¼ÓČėĒæ¼īČÜŅŗÖŠ£¬Ņ»øöµē¼«ĶØČėæÕĘų£¬ĮķŅ»µē¼«ĶØČė°±Ęų”£Ęäµē³Ų·“Ó¦ĪŖ4NH3£«3O2ØT2N2£«6H2O”£Š“³öøŗ¼«µē¼«·“Ó¦Ź½ ”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com