
| A、Cl2通入水中:Cl2+H2O=2H++Cl-+ClO- | ||||
B、用惰性电极电解饱和NaCl溶液:2H++2Cl-
| ||||
C、用石墨作电极电解CuSO4溶液:2Cu2++2H2O
| ||||
| D、钢铁发生吸氧腐蚀时负极反应为:Fe-3e-=Fe3+ |
| ||
| ||


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
| A、Na+ |
| B、SO42- |
| C、HCO3- |
| D、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
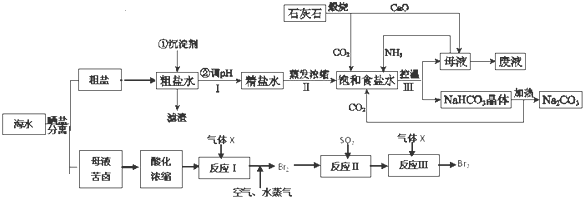
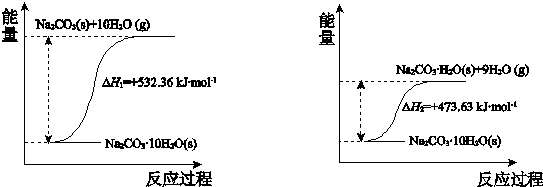
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1molS(s)完全反应,并转化为SO3(g)时,放出395.55kJ 热量 |
| B、1个SO2 和1个O2 分子储存的能量之和大于1个SO3 分子 |
| C、1LSO2 (g)完全反应生成1L SO3(g),放出98.32kJ 热量 |
| D、使用催化剂,可以减少反应②放出的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (4)
(4) (5)CH3COOH3(6)
(5)CH3COOH3(6)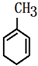 (7)
(7)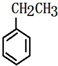 (8)
(8)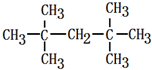 (9)
(9)
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、单位时间内生成了0.2molNH3的同时也生成了0.1mol N2 |
| B、3个H-H键断裂的同时有6个H-N键断裂 |
| C、混合气体的平均相对分子质量不再变化 |
| D、在该容器内,N2、H2、NH3浓度保持相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com