
下列实验方案中,不能测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的是
( )
A.取ag混合物充分加热,减重bg
B.取ag混合物与足量稀盐酸充分反应后,加热蒸干,灼烧,得bg固体
C.取ag混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重bg
D.取ag混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得bg固体
 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:
CH4和CO2反应可以制造价值更高的化学产品。
(1)250℃时,以镍合金为催化剂,向4 L容器中通入6 mol CO2、6 mol CH4,发生反应:CO2 (g)+CH4(g) 2CO(g)+2H2(g)。达到平衡时CH4的物质的量为2mol。
2CO(g)+2H2(g)。达到平衡时CH4的物质的量为2mol。
① 此温度下,该反应的平衡常数K=________(注明单位)。
② 保持温度不变,改变CH4和CO2的初始物质的量之比,充入容器进行反应,下列描述能够说明体系处于平衡状态的是 (填序号)。
a.容器内气体平均相对分子质量不随时间改变
b.混合气体的密度不随时间改变
c.单位时间内生成a mol CO2的同时消耗2a mol H2
d.混合气中n(CH4)∶n(CO2)∶n(CO)∶n(H2) =1∶1∶4∶4
③ 已知:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H1 kJ·mol-1
CO(g)+H2O (g)=CO2(g)+H2 (g) △H2 kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H3 kJ·mol-1
反应CO2(g)+CH4(g) 2CO(g)+2H2(g)的△H=_______________ kJ·mol-1
2CO(g)+2H2(g)的△H=_______________ kJ·mol-1
 (2)用Cu2Al2O4做催化剂,一定条件下,发生反应:
(2)用Cu2Al2O4做催化剂,一定条件下,发生反应:
CO2+CH4 CH3COOH,温度与催化剂的催化效率和乙酸的生成速率如图。250~300℃时,温度升高而乙酸的生成速率降低的原因是_________________________ __________。
CH3COOH,温度与催化剂的催化效率和乙酸的生成速率如图。250~300℃时,温度升高而乙酸的生成速率降低的原因是_________________________ __________。
(3)Li2O、Na2O、MgO均能吸收CO2,
①若寻找吸收CO2的其他物质,下列建议合理的是_________。
a. 可在碱性氧化物中寻找
b. 可在具有强氧化性的物质中寻找
 c. 可在ⅠA、ⅡA族元素的氧化物中寻找
c. 可在ⅠA、ⅡA族元素的氧化物中寻找
②Li4SiO4可用于吸收、释放CO2, 原理是: 500℃时,CO2与Li4SiO4接触生成Li2CO3;平衡后加热至700℃,反应逆向进行,放出CO2,Li4SiO4再生,该原理的化学方程式___________ ____________________________________。
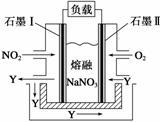
(4)以NO2、O2、熔融NaNO3组成的燃料电池装置如右图所示,在使用过程中石墨Ⅰ电极反应生成一种氧化物Y,有关电极反应可表示为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
向紫色石蕊试液中加入过量Na2O2粉末,振荡,正确的叙述是( )
①溶液为紫色 ②最后溶液变蓝色 ③最后溶液褪色 ④有气泡产生
A.①② B.②④ C.③④ D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
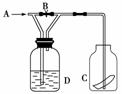
右图是一种试验某气体化学性质的实验装置,图中B为开关,如先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去。则D瓶中盛有的溶液是( )
A.浓H2SO4溶液
B.饱和NaCl溶液
C.浓NaOH溶液
D.浓Ba(OH)2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是( )
A.目前加碘食盐中主要添加的是KIO3
B.日常生活中无水乙醇常用于杀菌消毒
C.绿色食品是不含任何化学物质的食品
D.在空气质量日报中CO2含量属于空气污染指数
查看答案和解析>>
科目:高中化学 来源: 题型:
在一种酸性溶液中可能存在Fe3+、N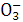 、Cl-、I-中的一种或几种,向该溶液中加入溴水,再加入淀粉,溶液变蓝。由此可推断溶液中( )
、Cl-、I-中的一种或几种,向该溶液中加入溴水,再加入淀粉,溶液变蓝。由此可推断溶液中( )
A.一定含有I-,不能 确定是否含有Cl-
确定是否含有Cl-
B.可能含有N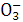 、Cl-和I-
、Cl-和I-
C.可能含有N
D.一定含有Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组为探索铜与浓硫酸的反应,用如图所示装置进行有关实验。
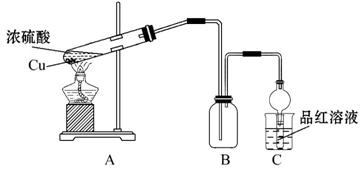
甲小组取ag铜片和一定量的浓硫酸放入试管中加热,直到反应完毕,最后发现试管中还有一定量的H2SO4和铜剩余。
(1)写出装置A中所发生反应的化学方程式____________________________。
(2)若用含0.2 mol H2SO4的浓硫酸与过量铜片共热,能否收集到0.1 mol SO2?________(填“能”或“不能”)。
(3)当集气瓶B中的气体收集满时,装置C中有可能观察到的现象是_________
_______________________________________________________________。
(4)为什么有一定量的余酸却未能使Cu完全溶解,你认为原因是_____ _____
_____ __
__
________________________________________________________________。
(5)乙组同学认为:实验装置C有可能造成环境污染,乙组学生设计了最简单方法给予解决:在C试管口塞上一团沾有________溶液的棉花。
(6)为了证明反应结束后的试管中的确有剩余的稀硫酸,可选择的试剂是________。
A.铁粉 B.Na2CO3溶液 C.BaCl2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子中,在碱性溶液里能大量共存,且溶液为无色透明的是
A. K+、MnO4-、Cl–、SO42- B. Na+、AlO2-、NO3-、CO32-
C. Na+、、H+、NO3-、SO42- D. Na+、SO32-、S2-、Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com