
化学与生产、生活密切相关.下列叙述正确的是
A.煤的干馏与石油的分馏均属于化学变化
B.BaSO4在医学上用作钡餐,Ba2+对人体无毒
C.14C可用于文物的年代鉴定, 14C与 13C互为同素异形体
D.葡萄糖注射液不能产生丁达尔现象,不属于胶体
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源:2016届吉林省长春十一高三下考前冲刺二理综化学试卷(解析版) 题型:选择题
A、B、C、D、E是原子序数依次增大的五种短周期元素且B、C相邻,A元素可以与B、C、E元素分别形成甲、乙、丙三种物质且甲、乙均为10电子化合物,丙为18电子化合物.D元素的最外层电子数与核外电子层数相等.已知:甲+E2=丙+B2,甲+丙=丁,下列说法正确的是( )
A.离子半径:D>C>B
B.A与B两种元素共同形成的10电子粒子有3种
C.D元素在周期表中的位置可以是第二周期第ⅡA族
D.丁物质均由非金属元素构成,只含共价键
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一下第三次考试化学试卷(解析版) 题型:选择题
某饱和一元醇C 7H15OH发生消去反应,只得到两种单烯烃,则该醇的结构简式可能是下列中的

查看答案和解析>>
科目:高中化学 来源:2016届海南省高三全真模拟二化学试卷(解析版) 题型:实验题
工业上常常利用物质的酸碱性分离混合物.某一混合物含苯酚、苯甲醇、苯甲酸和苯胺四种物质,其分离方案如图。
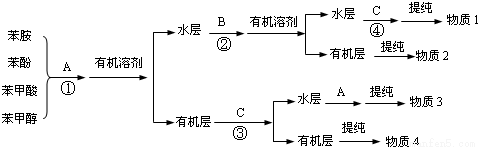
已知:①苯胺(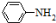 )有弱碱性,可与盐酸等反应生成盐;
)有弱碱性,可与盐酸等反应生成盐;
②常温下,苯胺、苯酚、苯甲酸、苯甲醇微溶于水,但均易溶于有机溶剂。
回答下列问题:
(1)写名称:物质2是 ,物质4是 。
(2)写出A、C的化学式:A , C 。
(3)写出反应②的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三全真模拟二化学试卷(解析版) 题型:选择题
硫酸亚铁隔绝空气加强热分解形成四氧化三铁,将分解生成的气体通入氯化钡溶液中,下列叙述正确的是
A.产生BaSO4沉淀? B.产生BaSO3沉淀?
C.产生BaSO4与BaSO3的混合沉淀 D.无沉淀产生
查看答案和解析>>
科目:高中化学 来源:2016届贵州省高三十二模理科化学试卷(解析版) 题型:简答题
随着化石能源的大量开采以及污染的加剧,污染气体的治理和开发利用日益迫切。
(1)Bunsen热化学循环制氢工艺由下列三个反应组成;
SO2(g) + I2(g) + 2H2O(g) = 2HI(g) + H2SO4(l) ∆H=a kJ/mol ①
2H2SO4(l) = 2H2O(g) + 2SO2(g) + O2(g) ∆H= b kJ/mol ②
2HI(g) = H2(g) + I2(g) ∆H= c kJ/mol ③
则2H2O(g) = 2H2(g) + O2(g) ∆H= kJ/mol
(2)CO2 和CH4 是两种重要的温室气体,以表面覆盖有Cu2Al2O4 的二氧化钛为催化剂。可以将CO2 和CH4直接转化为乙酸。

①不同温度下催化剂的催化效率与乙酸的生成速率如图Ⅰ所示,该反应体系应将温度控制在 ℃左右。
②将Cu2Al2O4 溶解在稀硝酸中的离子方程式为 。
(3)甲醇(CH3OH)被称为21世纪的新型燃料。在体积为V L的某反应容器中,a mol CO与2a mol H2 在催化剂作用下反应生成甲醇:CO(g) + 2H2(g)  CH3OH(g) ,CO的平衡转化率与温度的关系如图Ⅱ所示:
CH3OH(g) ,CO的平衡转化率与温度的关系如图Ⅱ所示:
①该反应是 (填“放热”或“吸热”)反应
②在其他条件不变的情况下,反应容器中再增加amol CO与2amolH2 ,达到新平衡时,CO的转化率 (填“增大”、“减小”或“不变”)。
③100℃,反应CH3OH(g)  CO(g) + 2H2(g) 的平衡常数为 (用含有a、V的代数表示)。
CO(g) + 2H2(g) 的平衡常数为 (用含有a、V的代数表示)。
(4)某实验小组设计了如图III所示的甲醇燃料电池装置。
①该电池工作时,OH- 向 (填“a”或“b”)极移动
②工作一段时间后,测得该溶液的pH减小,该电池负极反应的电极反应式为: 。
查看答案和解析>>
科目:高中化学 来源:2016届贵州省高三十二模理科化学试卷(解析版) 题型:选择题
设NA为阿伏伽德罗常数的值,下列说法正确的是 ( )
A.4.6g由NO2和N2O4组成的混合物中氧原子总数为0.2NA
B.标准状况下,22.4L的SO3中含3NA个氧原子。
C.100mL18.4mol/L的浓硫酸与足量的铜加热反应,转移的电子数为1.84NA
D.密闭的容器中,催化剂作用下0.5molN2与1.5molH2反应后得到NH3分子数一定为NA
查看答案和解析>>
科目:高中化学 来源:2016届甘肃西北师大附中高三下第五次诊断理科化学试卷(解析版) 题型:实验题
铝是人类生活中继铜、铁之后又一个重要的金属。工业上冶炼金属铝的原料来源于自然界中重要的矿物质钒土(主要成分:Al2O3;还有SiO2、Fe2O3、FeCO3、MgCO3等杂质)。从钒土中提取得到Al2O3的工艺流程如下图所示:

请回答下列问题:
(1)固体A所含物质的化学式(或分子式)是 。
(2)写出溶液A与足量气体B反应的离子方程式 。
(3)工业冶炼金属铝通常用石墨碳块作电解槽的阳极,请你根据电解原理解释电解冶炼铝的过程中,需要定期补充阳极碳块的原因 。
(4)Al2O3的熔点很高,因而在工业冶炼时,需将Al2O3熔于熔化的冰晶石(Na3AlF6)中进行电解。请写出电解过程中阴极的电极反应式 。工业上通常将Al(OH)3和Na2CO3一同溶于氢氟酸来制取冰晶石,反应时放出CO2气体,写出该反应的化学方程式 。
(5)有一位同学查阅资料发现,AlCl3的熔点很低。他提出:可通过电解熔融状态的AlCl3制取金属铝。你认为他提出的方案是否可行?为什么? 。
(6)某企业用上述工艺流程进行生产,每10.0t钒土可得到金属铝1.35t。如果不考虑生产过程的损耗,请你计算钒土中Al2O3的质量分数 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年北大附中河南分校高一下期末化学试卷(解析版) 题型:选择题
A、B、C、D、E是同周期元素,A、B的最高价氧化物的水化物呈碱性,且B比A的碱性强,C、D最高价氧化物水化物是酸,且C比D的酸性强,E是这五种元素中原子半径最大的,则它们的原子序数由小到大的顺序为( )
A. E、B、A、D、C B. D、B、C、A、E
C. E、C、D、B、A D. A、B、C、D、E
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com