
科目:高中化学 来源: 题型:
下列反应的离子方程式书写不正确的是( )
A.向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全:
Ba2++2OH-+H++ SO42- + NH4+= BaSO4↓+ NH3•H2O+H2O
B.氢氧化镁白色沉淀溶于氯化铵溶液:Mg(OH)2+2NH4+=Mg2++2NH3·H2O
C.硫化钠的水解:S2-+ 2H2O H2S + 2OH-
H2S + 2OH-
D.NaHCO3溶液中滴加少量澄清石灰水:2HCO3-+Ca2++2OH-= CaCO3↓+2H2O+ CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化合物的性质属于羟基对苯环影响的是
A.苯酚溶液显弱酸性
B.苯酚比苯容易发生溴代反应
C.苯酚能与NaOH溶液反应,而苯甲醇不能与NaOH溶液反应
D.苯酚和乙醇在60℃的水浴中,分别加入金属钠,苯酚中明显反应剧烈
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:
① 在稀碱溶液中,溴苯难发生水解
②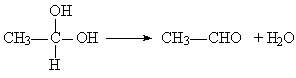
现有分子式为C10H10O2Br2的芳香族化合物X,其苯环上的一溴代物只有一种,其核磁共振氢谱图中有四个吸收峰,吸收峰的面积比为1:2:6:1,在一定条件下可发生下述一系列反应,其中C能发生银镜反应,E遇FeCl3溶液显色且能与浓溴水反应。
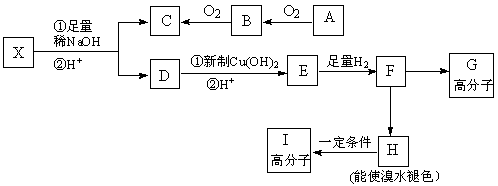

请回答下列问题:
(1)X中官能的名称是 。
(2)F→H的反应类型是 。
(3)I的结构简式为 。
(4)E不具有的化学性质 (选填序号)。
a.取代反应 b.消去反应 c.氧化反应 d.1molE最多能与2molNaHCO3反应
(5)写出下列反应的化学方程式:
① X与足量稀NaOH溶液共热的化学方程式: 。
② F→G的化学方程式: 。
(6)同时符合下列条件的E的同分异构体共有 种,其中一种的结构简式为 。
a.苯环上核磁共振氢谱有两种 b.不能发生水解反应
c.遇FeCl3溶液不显色 d.1molE最多能分别与1molNaOH和2molNa反应
查看答案和解析>>
科目:高中化学 来源: 题型:
在水溶液中能大量共存,且加入过量稀硫酸时,有气体生成的是( )
A. Na+、Ag+、CO32-、Cl- B. K+、 Ba2+、 SO42-、Cl-
C. Na+、K+、CO32-、Cl- D. Na+、K+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
某无色透明溶液可能存在Na+、Fe3+、Ba2+、NO3-、CO32-、HCO3-、SO42-中的几种离子,现有如下操作:
Ⅰ、取适量该溶液加入CaCl2溶液无沉淀,继续滴加盐酸产生无色无味的气体。
Ⅱ、另取该溶液滴加一定量的NaOH溶液有白色沉淀生成。
试回答下列问题:
该溶液中一定存在的离子有______________,一定不存在的离子_____________。
用一个离子方程式表示操作②的实验现象:
________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学用语或名称表达正确的是
A.亚硫酸的电离方程式:H2SO3 2H++SO
2H++SO
B.乙炔的分子结构模型示意图:
C.H2O2的电子式:
D. 的名称3-甲基-1-丁醇
的名称3-甲基-1-丁醇
查看答案和解析>>
科目:高中化学 来源: 题型:
 铝热反应是铝的一个重要性质,该性质用途十分广泛,不仅被用于焊接钢轨,而且还常被用于冶炼高熔点的金属如钒、铬、锰等。
铝热反应是铝的一个重要性质,该性质用途十分广泛,不仅被用于焊接钢轨,而且还常被用于冶炼高熔点的金属如钒、铬、锰等。
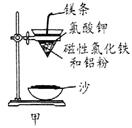
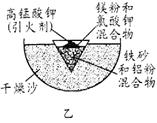

⑴ 某校化学兴趣小组同学,取磁性氧化铁按教材中的实验装置(如图甲)进行铝热反应,现象很壮观。取反应后的“铁块”溶于盐酸,向其中滴加KSCN溶液,发现溶液变血红色。出现这种现象的原因,除了可能混有没反应完的磁性氧化铁外,还有一个原因是 。
⑵ 若证明上述所得“铁块”中含有金属铝,可选择 (填试剂名称),所发生反应的离子方程式为 。
⑶ 为克服图甲的缺陷改用图乙装置进行铝热反应。取反应后的“铁块”溶于盐酸,向其中滴加KSCN溶液,溶液没有出现血红色。为测定该实验所得 “铁块”的成分,实验流程如图所示。
 |
几种氢氧化物开始沉淀和完全沉淀的pH如下表所示。
| Fe2+ | Fe3+ | Al3+ | Mg2+ | |
| 开始沉淀时的pH | 7.5 | 2.8 | 4.2 | 9.6 |
| 沉淀完全时的pH | 9.0 | 4.0 | 5 | 11 |
① 试剂A应选择 ,试剂B应选择 。(填序号)
A.稀盐酸 B.氧化铁 C.H2O2溶液 D.氨水 E.MgCO3固体
② 已知常温下Fe(OH)3的Ksp=1.1×10-36,则反应Ⅲ后溶液中c(Fe3+)= mol·L-1。
③ 灼烧完全的标志是 。
④ 若最终红色粉未M的质量为12.0 g,则该“铁块”的纯度是 。如果对所得过滤固体直接洗涤、烘干、称量,计算“铁块”的纯度,则计算结果会 (填“偏大”“偏小”或“无影响”),原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:HCN(aq)与NaOH(aq)反应的Δ H=-12.1 kJ·mol-1;HCl(aq)与NaOH(aq)
H=-12.1 kJ·mol-1;HCl(aq)与NaOH(aq)
反应的ΔH=-55.6 kJ·mol-1。则HCN在水溶液中电离的ΔH等于( )
A.-67.7 kJ·mol-1 B.-43.5 kJ·mol-1
C.+43.5 kJ·mol-1 D.+67.7 kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com