
【题目】下列判断正确的是
A.常温下,将等物质的量浓度的氨水与盐酸混合,当溶液呈中性时,所加的两溶液的体积恰好相等
B.常温下,NaAc溶液的PH等于8,则![]()
C.常温下,![]() 的
的![]() 溶液和
溶液和![]() 的
的![]() 溶液中,水的电离程度是:前者大于后者
溶液中,水的电离程度是:前者大于后者
D.常温下,![]() 的
的![]() 溶液中,
溶液中,![]()
科目:高中化学 来源: 题型:
【题目】现代火法炼锌过程中发生了以下三个主要反应。下列说法正确的是( )
① 2ZnS(s) + 3O2(g)=2ZnO(s)+2SO2(g) △H1=a kJ·mol-1
② 2C(s) +O2(g)=2CO(g) △H2=b kJ·mol-1
③ ZnO(s) +CO(g)=Zn(g) +CO2(g) △H3=c kJ·mol-1
A.以上三个反应中,只有①是放热反应
B.反应②的作用是仅为反应③提供还原剂
C.反应 ZnS(s)+C(s)+2O2(g)=Zn(g)+SO2(g)+CO2(g)的△H=![]() (a+b+2c) kJ·mol-1
(a+b+2c) kJ·mol-1
D.碳的燃烧热为![]() b kJ·mol-1
b kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20mL某一元酸(HA)溶液中逐滴加入0.1mol·L-1的NaOH溶液,测得混合溶液中由水电离出的c(H+)随加入NaOH溶液的体积变化关系图如下。下列说法不正确的是

A. Ka(HA)的数量级为10-5
B. d点溶液的pH最大
C. b点溶液显酸性,c(A-)>c(Na+)>c(H+)>c(OH-)
D. d点溶液中,c(Na+)+c(H+)=c(A-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】测定0.1 mol·L-1 Na2SO3溶液先升温再降温过程中的pH,数据如下。
时刻 | ① | ② | ③ | ④ |
温度/℃ | 25 | 30 | 40 | 25 |
pH | 9.66 | 9.52 | 9.37 | 9.25 |
实验过程中,取①④时刻的溶液,加入盐酸酸化的BaCl2溶液做对比实验,④产生白色沉淀多。
下列说法不正确的是
A. Na2SO3溶液中存在水解平衡:![]() +H2O
+H2O![]()
![]() +OH
+OH
B. ④的pH与①不同,是由于![]() 浓度减小造成的
浓度减小造成的
C. ①→③的过程中,温度和浓度对水解平衡移动方向的影响一致
D. ①与④的Kw值相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中存在如下反应:2SO2 (g)+O2 (g)![]() 2SO3(g) ΔH<0。某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析不正确的是( )
2SO3(g) ΔH<0。某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析不正确的是( )
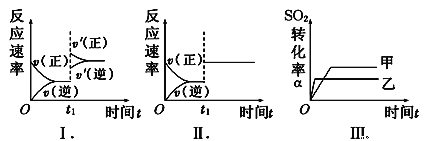
A.图Ⅰ表示的是t1时刻增大压强对反应速率的影响
B.图Ⅱ表示的是t1时刻加入催化剂对反应速率的影响
C.图Ⅲ表示的是压强对化学平衡的影响,且P甲大于P乙
D.图Ⅲ表示的是温度对化学平衡的影响,且T甲小于T乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示溶液中c(H+)和c(OH-)的关系,下列判断错误的是
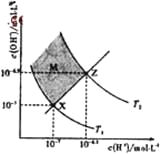
A. 两条曲线间任意点均有c(H+)×c(OH-)=Kw
B. M区域内任意点均有c(H+)<c(OH-)
C. 图中T1<T2
D. XZ线上任意点均有pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知水中存在如下平衡:H2O+H2O![]() H3O++OH- ΔH>0,现欲使平衡向右移动,且所得溶液呈酸性,选择的方法是( )
H3O++OH- ΔH>0,现欲使平衡向右移动,且所得溶液呈酸性,选择的方法是( )
A.加热水至100℃[其中c(H+)=1×10-6mol·L-1]B.向水中加入NaHSO4
C.向水中加入Cu(NO3)2D.在水中加入Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化)。下列各组物质中,满足图示转化关系的是( )
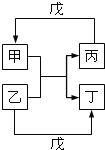
物质 选项 | 甲 | 乙 | 丙 | 戊 | 丁 |
A | Cu | HNO3 | Cu(NO3)2 | Fe | NO |
B | H2O | Fe | H2 | O2 | Fe2O3 |
C | Al | NaOH | H2 | Al2O3 | NaAlO2 |
D | CH3CHO | O2 | CH3COOH | H2 | H2O |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组数据中,前者刚好是后者两倍的是( )
A.2mol水的摩尔质量和1mol水的摩尔质量
B.200mL1mol/L氯化钙溶液中c(Cl-)和100mL2mol/L氯化钾溶液中c(Cl-)
C.32g二氧化硫中氧原子数和标准状况下11.2L一氧化碳中氧原子数
D.20%NaOH溶液中NaOH的物质的量浓度和10%NaOH溶液中NaOH的物质的量浓度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com