
| A.蒸馏法 | B.过滤法 | C.电渗析法 | D.离子交换法 |
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源:不详 题型:单选题
| A.用NaOH溶液除去CO2中混有的SO2 |
| B.将混合气体通过灼热的铜网除去N2中的少量O2 |
| C.用新制的生石灰,通过加热蒸馏,以除去乙醇中的少量水 |
| D.用盐酸除去AgCl中少量的Ag2CO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:多选题
| A.除去Mg粉中的Al粉:加入足量NaOH溶液后,过滤、洗涤 |
| B.除去BaCO3固体中混有的BaSO4:加过量盐酸后,过滤、洗涤 |
| C.除去NaHCO3溶液中Na2CO3:加适量稀盐酸 |
| D.除去FeCl2溶液中混有的FeCl3:加入过量铁粉,过滤 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 CO(NH2)2·H2O2。过氧化尿素的部分性质如下:
CO(NH2)2·H2O2。过氧化尿素的部分性质如下:| 分子式 | 外观 | 热分解温度 | 熔点 | 溶解性 |
| CO(NH2)2?H2O2 | 白色晶体 | 45℃ | 75~85℃ | 易溶于水、有机溶剂 |

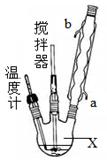
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.制乙酸乙酯时,迅速将乙醇注入浓硫酸中 |
| B.在石油蒸馏装置中,将温度计水银球插入液面以下 |
| C.用铂丝蘸取少量KCl溶液置于火焰上灼烧,直接观察火焰颜色,检验K+的存在 |
| D.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Fe3+和Cl- | B.Na+和SO42- | C.Fe3+和SO42- | D.Na+和Cl- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.乙酸和乙酸乙酯可用Na2CO3溶液加以区别 |
| B.戊烷(C5H12)有两种同分异构体 |
| C.乙烯、聚氯乙烯和苯分子均含有碳碳双键 |
| D.糖类、油脂和蛋白质均可发生水解反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com