
三氯化磷(PCl3)是一种重要的半导体材料掺杂剂。实验室要用黄磷(白磷)与干燥的Cl2模拟工业生产制取PCl3,装置如图所示。
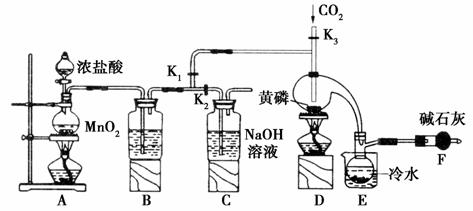
已知:PCl3遇O2会生成POCl3,POCl3能溶于PCl3,且PCl3遇水会强烈水解生成H3PO3和HCl。PCl3、POCl3的熔沸点见下表。
| 物质 | 熔点/℃ | 沸点/℃ |
| PCl3 | -112 | 75.5 |
| POCl3 | 2 | 105.3 |
请回答下列问题:
(1)A中制氯气的离子方程式为________________。
(2)B中所装试剂是________________。
(3)E中冷水的作用是________________。
(4)实验时,检查装置气密性后,先打开K3通入干燥的CO2,再迅速加入黄磷。通入干燥CO2的作用是________________。
(5)粗产品中常含有POCl3、PCl5等。加入黄磷加热除去PCl5后,通过________________(填实验操作名称),即可得到较纯净的PCl3。
解析:本题考查了PCl3制取的有关知识,意在考查考生对化学实验知识的掌握情况。(1)由实验装置图可知,A中加的药品为二氧化锰和浓盐酸,所以发生的反应为MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,离子方程式为MnO2+4H++2Cl-
MnCl2+Cl2↑+2H2O,离子方程式为MnO2+4H++2Cl- Mn2++Cl2↑+2H2O。(2)~(4)B中装有浓硫酸,干燥氯气,C是尾气吸收装置,D装置进行氯气与磷的反应,因为PCl3沸点低,为防止其挥发,将装置E放入冷水中,通入干燥CO2的目的是排尽装置中的空气,防止黄磷自燃。(5)加入黄磷加热除去PCl5后,通过蒸馏即可得到较纯净的PCl3。
Mn2++Cl2↑+2H2O。(2)~(4)B中装有浓硫酸,干燥氯气,C是尾气吸收装置,D装置进行氯气与磷的反应,因为PCl3沸点低,为防止其挥发,将装置E放入冷水中,通入干燥CO2的目的是排尽装置中的空气,防止黄磷自燃。(5)加入黄磷加热除去PCl5后,通过蒸馏即可得到较纯净的PCl3。
答案:(每空2分)(1)MnO2+4H++2Cl-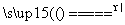 Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
(2)浓硫酸
(3)防止PCl3挥发(冷凝)
(4)排尽装置中的空气,防止黄磷(白磷)自燃
(5)蒸馏


科目:高中化学 来源: 题型:
工业制取硫酸有一步重要反应是SO2在400~5000C下的催化氧化,2SO2+O2 2SO3,这是一个正反应放热的可逆反应,如果反应在密闭容器中进行,下述有关说法中错误的是 ( )
2SO3,这是一个正反应放热的可逆反应,如果反应在密闭容器中进行,下述有关说法中错误的是 ( )
A、使用催化剂是为了加快反应速率,提高生产效率
B、在上述条件下,SO2不可能100%的转化为SO3
C、达到平衡时,SO2的浓度与SO3的浓度相等
D、为了提高SO2的转化率,应适当提高O2的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验装置进行的相应实验,能达到实验目的的是( )

A.图①除去CO2中的HCl
B.图②装置制备Fe(OH)2并能较长时间观察其颜色
C.图③装置可用于分离C2H5OH和H2O的混合物
D.图④证明CH3CH2OH发生消去反应生成了乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
PM2.5是指大气中直径小于或等于2.5微米的颗粒物,是灰霾天气的主要原因,它主要来自化石燃料的燃烧(如机动车尾气、燃煤)等,下列与PM2.5相关的说法不正确的是( )
A.大力发展电动车,减少燃油汽车的尾气排放量
B.开发利用各种新能源,减少对化石燃料的依赖
C.多环芳烃是强致癌物,能吸附在PM2.5的表面进入人体
D.PM2.5含有的铅、镉、铬、钒、砷等对人体有害的元素均是金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
现有如下仪器,仪器中已注入溶液,回答下列问题。

(1)加热装置A,写出铜与浓硫酸反应的化学方程式:_________,烧瓶中的实验现象为________________。
(2)验证碳、硅非金属性的相对强弱(已知酸性:H2SO3>H2CO3),若选择仪器A、B、C、D并相连接,则B、C、D中所选择的试剂为B________________、C________________、D________________。能说明碳的非金属性比硅强的实验现象是________________。
(3)验证SO2的氧化性、还原性。若选择A、E、F仪器,并按A、E、F顺序连接。
①则证明SO2有氧化性的实验现象是_____________________,反应方程式为__________________________。
②若证明SO2具有还原性,在E中采取的实验操作为_________,其实验现象为________________,反应原理为________________(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中发生反应: aX(g)+bY(g) 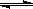 cZ(g)+dW(g)反应达到平衡后,将气体体积压缩到
cZ(g)+dW(g)反应达到平衡后,将气体体积压缩到
原来的一半,当再次达到平衡时,W的浓度为原平衡状态的1.8倍。下列叙述正确的是( )
A.平衡向正反应方向移动 B.(a+b)>(c+d)
C.Z的体积分数变大 D.X的转化率变小
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述错误的是( )
A.用新制的银氨溶液可区分甲酸甲酯和乙醛
B.用高锰酸钾酸性溶液可区分己烷和3-己烯
C.用水可区分苯和溴苯
D.用金属钠可区分乙醇和乙醚
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各项表达中,正确的是
A.水的电子式为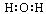
B.将58g等体积的乙烯和乙烷混合物完全燃烧,生成的二氧化碳体积为89.6L
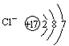 C.所有的氮原子中,质子数都是7个,但不一定是相同的原子
C.所有的氮原子中,质子数都是7个,但不一定是相同的原子
D.氯离子的结构示意图为
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上常利用含硫废水生产Na2S2O3•5H2O,实验室可用如下装置(略去部分加持仪器)模拟生成过程。
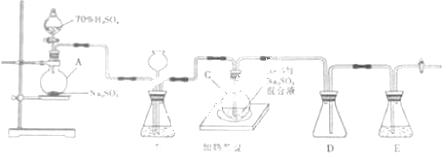
烧瓶C中发生反应如下:
Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq) (I)
2H2S(aq)+SO2(g)=3S(s)+2H2O(l) (II)
S(s)+Na2SO3(aq)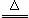 Na2S2O3(aq) (III)
Na2S2O3(aq) (III)
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液注,若 ,则整个装置气密性良好。装置D的作用是
。装置E中为 溶液。
(2)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为  。
。
(3)装置B的作用之一是观察SO2的生成速 率,其中的液体最好选择 。
率,其中的液体最好选择 。
a.蒸馏水 b.饱和Na2SO3溶液
c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
实验中,为使SO2缓慢进入烧瓶C,采用的操作是 。已知反应(III)相对较慢,则烧瓶C中反应达到终点的现象是 。反应后期可用酒精灯适当加热烧瓶A,实验室用酒精灯加热时必须使用石棉网的仪器含有 。
a.烧杯 b.蒸发皿 c.试管 d.锥形瓶
(4)反应终止后,烧瓶C中的溶液经蒸发浓缩即可析出Na2S2O3•5H2O,其 中可能含有Na2SO3、Na2SO4等杂质。利用所给试剂设计实验,检测产品中是否存在Na2SO4,简要说明实验操作,现象和结论:
中可能含有Na2SO3、Na2SO4等杂质。利用所给试剂设计实验,检测产品中是否存在Na2SO4,简要说明实验操作,现象和结论:
。
已知Na2S2O3•5H2O遇酸易分解:S2O32‾+2H+=S↓+SO2↑+H2O
供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com