
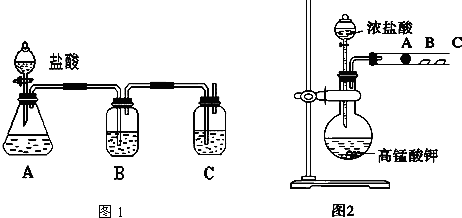
分析 (1)图1是比较非金属性强弱,元素的非金属性越强,其最高价氧化物的水化物酸性越强,强酸能和弱酸盐反应生成弱酸,所以图1中用A制取二氧化碳,用B洗气,用C装置检验碳酸和硅酸酸性强弱;
(2)图2实验目的是比较卤族元素性质递变规律,元素的非金属性越强,其单质的氧化性越强,要检验氧化性强弱顺序:Cl2>Br2>I2,根据卤素单质之间的置换反应判断即可,据此分析解答.
解答 解:(1)图1是比较非金属性强弱,元素的非金属性越强,其最高价氧化物的水化物酸性越强,强酸能和弱酸盐反应生成弱酸,所以图1中用A制取二氧化碳,盐酸具有挥发性,所以生成的二氧化碳中含有HCl,HCl也能和硅酸钠反应生成硅酸,为防止HCl干扰实验,用B洗气,用C装置检验碳酸和硅酸酸性强弱,则A中盛放试剂是Na2CO3溶液、B中盛放试剂是饱和的NaHCO3溶液、C中盛放试剂是硅酸钠溶液;
故答案为:Na2CO3溶液;饱和的NaHCO3溶液;硅酸钠溶液;除去二氧化碳中的杂质HCl;
(2)图2实验目的是比较卤族元素性质递变规律,元素的非金属性越强,其单质的氧化性越强,要检验氧化性强弱顺序:Cl2>Br2>I2,根据卤素单质之间的置换反应判断即可,
氯气和NaBr发生置换反应生成红棕色物质溴,离子反应方程式为Cl2+2Br-=Br2+2Cl-;
溴和KI反应生成紫色物质碘,碘遇淀粉试液变蓝色,所以B处试纸显蓝色;
氯气、溴和碘都毒,不能直接排空,用NaOH吸收,防止污染空气,
故答案为:Cl2+2Br-=Br2+2Cl-;试纸变蓝色;处理尾气.
点评 本题考查性质实验方案设计,为高频考点,明确实验原理及物质性质性质是本题关键,注意物质检验时要排除其它物质的干扰,知道常见元素化合物性质,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 1 mol O2与Na完全反应,转移电子数一定为4NA | |
| B. | 22.4 L NH3中含有共价键的数目为3NA | |
| C. | 142 g Na2SO4和Na2HPO4混合物中含有的阴、阳离子总数是3NA | |
| D. | 标准状况下,11.2 L SO3所含的分子数目为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴乙烷$\stackrel{AgNO_{3}溶液}{→}$浅黄↓ | |
| B. | 溴乙烷$→_{HNO_{3}}^{AgNO_{3}}$浅黄↓ | |
| C. | 溴乙烷$→_{△}^{NaOH和水}$$→_{AgNO_{3}溶液}^{HNO_{3}}$浅黄↓ | |
| D. | 溴乙烷$→_{△}^{NaOH和乙醇}$$\stackrel{AgNO_{3}溶液}{→}$浅黄↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com