
【题目】NA为阿伏加德罗常数的数值,下列说法正确的是( )
A. 7.2 g CaO2晶体中阴离子和阳离子总数为0.3 NA
B. 0.1 mol/L NH4Cl溶液中Cl-离子数目为0.1 NA
C. 反应3H2(g)+N2(g)![]() 2NH3(g) ΔH=-92 kJ/mol,放出热量9.2 kJ时,转移电子0.6 NA
2NH3(g) ΔH=-92 kJ/mol,放出热量9.2 kJ时,转移电子0.6 NA
D. 0.1 mol H2O2分子中含极性共价键数目为0.3 NA
科目:高中化学 来源: 题型:
【题目】下列广告用语在科学上没有错误的是 ( )
A.这种饮料中不含任何化学物质
B.这种蒸馏水绝对纯净,其中不含任何离子
C.这种口服液含丰富的氮、磷、锌等微量元素
D.没有水就没有生命
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去混在甲烷中的二氧化碳和水蒸气,可将混合气体先通过盛有__________(填物质名称,下同)的洗气瓶除去__________;再通过盛有__________的洗气瓶除去________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
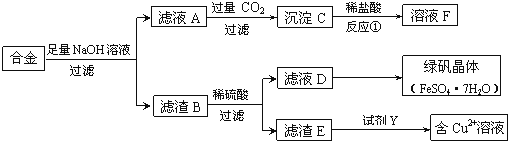
(1)合金与足量氢氧化钠溶液反应的离子方程式是 。
(2)若D中含有Fe3+,除去Fe3+的常用试剂是 。
(3)若要从滤液D中得到绿矾晶体,必须进行的实验操作步骤: 、冷却结晶、过滤、自然干燥。
(4)若由滤渣E得到含Cu2+的溶液,试剂Y可能是 (填选项字母)。
A.稀硝酸 | B.浓硫酸 | C.浓盐酸 | D.稀硫酸 |
根据所选试剂写出一个由滤渣E得到含Cu2+溶液的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6g。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示(己知硝酸只被还原为NO气体)。下列分析或结果错误的是
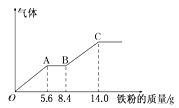
A. H2SO4浓度为2.5mol·L-1
B. OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气
C. 第二份溶液中最终溶质为FeSO4
D. 原混合酸中NO3-的物质的量为0.1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:A是石油裂解气的主要成份,能使溴水褪色;A是一种重要的化工原料,它的产量通常用来衡量一个国家石油化工水平.现以A为主要原料合成乙酸乙酯及高分子化合物E,其合成路线如图所示:

请回答下列问题:
(1)写出A的电子式 .
(2)B、D分子中的官能团名称分别是 、 .
(3)写出下列反应的化学方程式并指出反应类型:
① 反应类型 ;
② 反应类型 ;
④ 反应类型 。
⑤ 反应类型 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关非金属元素说法正确的是
A.二氧化氯具有还原性,可用于自来水的杀菌消毒
B.液氨汽化时要吸收大量的热,可用作制冷剂
C.硫具有还原性,可用硫粉覆盖地上洒落的汞
D.硅是重要的半导体材料,常用于制作光导纤维
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组进行实验探究:探究碳、硅元素的非金属性的相对强弱。实验装置如下,请根据要求回答下列问题:
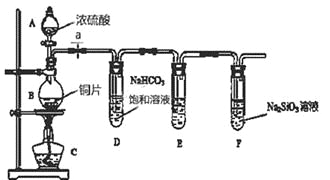
(1)填写所示仪器名称:A 。
(2)实验步骤:连接仪器、 、加药品后,打开a、然后滴入浓硫酸,加热。
(3)问题探究:(已知酸性强弱:亚硫酸 >碳酸)
①铜与浓硫酸反应的化学方程式是 ;装置E中盛足量酸性KMnO4溶液的作用是 。
②该实验证明碳元素的非金属性比硅元素非金属性强的实验依据是 。
③依据试管D中发生的反应,能否证明硫元素的非金属性强于碳元素的非金属性 (填“能”或“否”),原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com