
【题目】室温下,将1.000 mol·L-1盐酸滴入20.00 mL 1.000 mol·L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如下图所示。下列有关说法正确的是
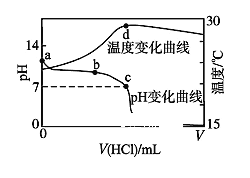
A. a点由水电离出的c(OH-)=1.0×10-14 mol·L-1
B. b点:c(NH4+)+c(NH3·H2O)=c(Cl-)
C. c点:c(Cl-)>c(NH4+)
D. d点:达到滴定终点
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】(1)常温下,在200 mL氢氧化钡溶液中含有1×10-3mol的钡离子,将此溶液与pH=3的盐酸混合,使其混合溶液的pH=7,应取氢氧化钡溶液和盐酸的体积之比是_________。
(2)25℃时,利用pH试纸测得0.1molL-1醋酸溶液的pH约为3,则可以估算出醋酸的电离常数约为_______;向10mL此溶液中加入少量冰醋酸,忽略溶解过程中溶液温度和体积的微小变化,溶液中c(H+)/c(CH3COOH)的值将_____(填“增大”、“减小”或“无法确定”)。
(3)25 ℃时,pH=3的NH4Al(SO4)2中2c(SO42-)-c(NH4+)-3c(Al3+)=______(取近似值)
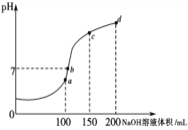
(4)室温时,向100mL0.1mol·L-1NH4HSO4溶液中滴加0.1mol·L-1NaOH溶液,溶液pH与NaOH溶液体积的关系曲线如图所示:试分析图中a、b、c、d四个点,水的电离程度最大的是________点;在b点,溶液中各离子浓度由大到小的排列顺序是__________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+B(g) ![]() 2C(g) ΔH<0,达到平衡时,下列说法正确的是
2C(g) ΔH<0,达到平衡时,下列说法正确的是
A. 加入催化剂,B的转化率增大 B. 减小容器体积,平衡不移动
C. 增大c(A),A的转化率增大 D. 降低温度,v正 增大,v逆 减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2,4二氯苯乙酸是生产新型杀虫、杀螨剂螺螨酯的关键中间体,其结构简式如图所示。下列有关说法错误的是( )
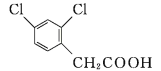
A. 该有机物能发生加成反应、取代反应
B. 该有机物的分子式为C8H6Cl2O2
C. 改变氯原子在苯环上的位置,还可得到8种结构
D. 该有机物分子中所有的碳原子可能同时处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业采用氯化铵焙烧菱锰矿制备高纯碳酸锰的流程如图所示:

已知:①菱锰矿的主要成分是MnCO3,其中含Fe、Ca、Mg、Al等元素。
②Al3+、Fe3+沉淀完全的pH分别为4.7、3.2,Mn2+、Mg2+开始沉淀的pH分别为8.1、9.1。
③焙烧过程中主要反应为MnCO3+2NH4Cl![]() MnCl2+2NH3↑+CO2↑+H2O。
MnCl2+2NH3↑+CO2↑+H2O。
(1)结合图1、2、3,分析焙烧过程中最佳的焙烧温度、焙烧时间、![]() 分别为_____、_____、_______。
分别为_____、_____、_______。

(2)对浸出液净化除杂时,需先加入MnO2将Fe2+转化为Fe3+,再调节溶液pH的范围为_______,将Fe3+和Al3+变为沉淀而除去,然后加入NH4F将Ca2+、Mg2+变为氟化物沉淀除去。
(3)“碳化结晶”步骤中,加入碳酸氢铵时反应的离子方程式为______________。
(4)上述流程中可循环使用的物质是________。
(5)现用滴定法测定浸出液中Mn2+的含量。实验步骤:称取1.000 g试样,向其中加入稍过量的磷酸和硝酸,加热使反应2Mn2++![]() +4
+4![]() +2H+
+2H+![]() 2[Mn(PO4)2]3+
2[Mn(PO4)2]3+![]() +H2O充分进行;加入稍过量的硫酸铵,发生反应
+H2O充分进行;加入稍过量的硫酸铵,发生反应![]() +
+![]()
![]() N2↑+2H2O以除去
N2↑+2H2O以除去![]() ;加入稀硫酸酸化,用2.00 mol·L110.00 mL硫酸亚铁铵标准溶液进行滴定,发生的反应为[Mn(PO4)2]3+Fe2+
;加入稀硫酸酸化,用2.00 mol·L110.00 mL硫酸亚铁铵标准溶液进行滴定,发生的反应为[Mn(PO4)2]3+Fe2+![]() Mn2++ Fe3++2
Mn2++ Fe3++2![]() ;用0.10 mol·L110.00 mL酸性K2Cr2O7溶液恰好除去过量的Fe2+。
;用0.10 mol·L110.00 mL酸性K2Cr2O7溶液恰好除去过量的Fe2+。
①酸性K2Cr2O7溶液与Fe2+反应的离子方程式为_____________(还原产物是Cr3+)。
②试样中锰的质量分数为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中,A是固体金属单质,燃烧时火焰呈黄色,B为淡黄色固体。请回答下列问题:

(1)写出下列转化的化学方程式:
B→D_____。
A→C_____。
B→C_____。
(2)写出B物质的一种重要用途___。
(3)A的保存方法是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.2 mol/L的KI溶液和0.01mol/L Fe2(SO4)3溶液等体积混合后,取混合液分别进行实验。下列能说明溶液中存在平衡2Fe3++2I-![]() 2Fe2++I2的是
2Fe2++I2的是
A. 滴入硝酸银溶液产生黄色沉淀 B. 加入酸性KMnO4溶液,溶液紫红色褪去
C. 滴入淀粉溶液,溶液变蓝色 D. 滴入KSCN溶液,溶液变红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应2NO2(g) ![]() N2O4(g) ΔH=-57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的为( )
N2O4(g) ΔH=-57kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的为( )

A. A、C两点气体的颜色:A深,C浅
B. A、C两点的反应速率:A>C
C. A、C两点气体的平均相对分子质量:A>C
D. 由状态A到状态B,可以采用降温的方法
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com