
某校化学实验兴趣小组欲采用如图所示的实验装置制备Cl2,同时进行与氯气有关的某些实验,按要求回答问题。
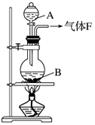
(1)A是浓盐酸,B是二氧化锰,将A滴入B中时发生反应的离子方程式为______________。
(2)甲同学用含有0.2 mol HCl的浓盐酸与足量的MnO2反应制Cl2,结果制得的Cl2体积在标准状况下小于1.12 L,这是由于反应过程中盐酸浓度变小造成的。请列举导致盐酸浓度变小的原因:__________。
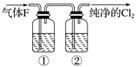
(3)在实验室中,乙同学欲用下图中的装置净化氯气,则瓶①②中应盛放的试剂分别是①__________,②______(填试剂名称)。
(4)丙同学将纯净的Cl2通入一定量石灰乳中来制取漂白粉,若通入224 mL标准状况下Cl2完全反应时,则反应过程中转移电子的物质的量为________。
答案 (1)MnO2+4H++2Cl-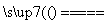 Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
(2)氯化氢挥发;反应生成水;反应消耗HCl
(3)饱和食盐水 浓硫酸
(4)0.01 mol
解析 (1)二氧化锰氧化浓盐酸可以制取氯气,离子方程式为MnO2+4H++2Cl-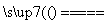 Mn2++Cl2↑+2H2O。(2)浓盐酸浓度变小是因为二氧化锰和浓盐酸反应过程中消耗HCl,加热时氯化氢挥发,生成的水稀释浓盐酸。(3)制取的氯气中含有氯化氢和水蒸气,净化时应先通过饱和食盐水吸收氯化氢,后通过浓硫酸吸收水蒸气。(4)反应2Ca(OH)2+2Cl2===CaCl2+Ca(ClO)2+2H2O中,1 mol Cl2参加反应转移1 mol电子,故通入224 mL标准状况下Cl2完全反应时,反应过程中转移电子0.01 mol。
Mn2++Cl2↑+2H2O。(2)浓盐酸浓度变小是因为二氧化锰和浓盐酸反应过程中消耗HCl,加热时氯化氢挥发,生成的水稀释浓盐酸。(3)制取的氯气中含有氯化氢和水蒸气,净化时应先通过饱和食盐水吸收氯化氢,后通过浓硫酸吸收水蒸气。(4)反应2Ca(OH)2+2Cl2===CaCl2+Ca(ClO)2+2H2O中,1 mol Cl2参加反应转移1 mol电子,故通入224 mL标准状况下Cl2完全反应时,反应过程中转移电子0.01 mol。


 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:高中化学 来源: 题型:
氢化亚铜(CuH)是一难溶物质,用CuSO4溶液和另一种“反应物”在40~50 ℃时反应可生成它。CuH不稳定,易分解;CuH在氯气中能燃烧,跟盐酸反应能产生气体。下列有关推断中错误的是( )
A.这里的“另一种反应物”具有还原性
B.CuH可作氧化剂、还原剂
C.CuH+Cl2 CuCl+HCl
CuCl+HCl
D.CuH+HCl===CuCl+H2↑(常温)
查看答案和解析>>
科目:高中化学 来源: 题型:
将氯水分别滴入下列各选项所述的溶液中,由实验现象得出的结论完全正确的是( )
| 选项 | 氯水滴入下列溶液中 | 实验现象 | 结论 |
| A | 滴有KSCN的FeCl2溶液 | 变血红 | Cl2具有还原性 |
| B | 滴有酚酞的NaOH溶液 | 褪色 | Cl2具有漂白性 |
| C | 紫色石蕊溶液 | 先变红后褪色 | Cl2具有酸性、漂白性 |
| D | KI淀粉溶液 | 变蓝色 | Cl2具有氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
NaCl是一种化工原料,可以制备一系列物质(见下图)。下列说法正确的是( )

A.25 ℃,NaHCO3在水中的溶解度比Na2CO3的大
B.石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂
C.常温下干燥的Cl2能用钢瓶贮运,所以Cl2不与铁反应
D.图中所示转化反应都是氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组的同学利用MnO2、浓盐酸反应来制取干燥的氯气并验证其有无漂白性,所用装置如图所示(可重复使用,不含制气装置)。下列说法正确的是( )
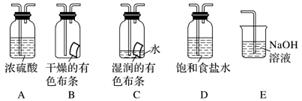
A.按气流流动的先后顺序,装置连接顺序依次为DACBE
B.按气流流动的先后顺序,装置连接顺序依次为DABAE
C.装置E的主要用途是制备NaClO
D.若实验中使用到装置C且有色布条褪色,则说明湿润的氯气有漂白性
查看答案和解析>>
科目:高中化学 来源: 题型:
实验证明,多数能自发进行的反应都是放热反应。对此说法的理解正确的是( )
A.所有的放热反应都是自发进行的
B.所有的自发反应都是放热的
C.焓变是影响反应是否具有自发性的一种重要因素
D.焓变是决定反应是否具有自发性的唯一判据
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中进行反应:X2(g)+Y2(g)2Z(g),已知X2、Y2、Z的起始浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.2 mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )
A.Z为0.3 mol·L-1 B.Y2为0.4 mol·L-1
C.X2为0.2 mol·L-1 D.Z为0.4 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
在10 L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)M(g)+N(g),所得实验数据如下表:
| 实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
| n(X) | n(Y) | n(M) | ||
| ① | 700 | 0.40 | 0.10 | 0.090 |
| ② | 800 | 0.10 | 0.40 | 0.080 |
| ③ | 800 | 0.20 | 0.30 | a |
| ④ | 900 | 0.10 | 0.15 | b |
下列说法正确的是( )
A.实验①中,若5 min时测得n(M)=0.050 mol,则0至5 min 时间内,用N表示的平均反应速率v(N)=1.0×10-2 mol·L-1·min-1
B.实验②中,该反应的平衡常数K=2.0
C.实验③中,达到平衡时,X的转化率为60%
D.实验④中,达到平衡时,b>0.060
查看答案和解析>>
科目:高中化学 来源: 题型:
以下微粒含配位键的是( )
①N2H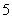 ②CH4 ③OH- ④NH
②CH4 ③OH- ④NH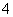 ⑤Fe(CO)3
⑤Fe(CO)3
⑥Fe(SCN)3 ⑦H3O+ ⑧[Ag(NH3)2]OH
A.①②④⑦⑧ B.③④⑤⑥⑦
C.①④⑤⑥⑦⑧ D.全部
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com