
分析 (1)CCl4从碘水中萃取碘并用分液漏斗分离两种溶液,操作为查漏→装液→振荡→静置→分液;
(2)旋开活塞,分离下层液体,应使漏斗下端管口紧靠烧杯内壁,及时关闭活塞,(G)步骤可使液体顺利流下;
(3)碘在水、四氯化碳中的溶解性不同;
(4)萃取剂的选择原则有三条:一是溶质在萃取剂中的溶解度比在水中要大得多;二是萃取剂与水互不溶解能分成两层;三是萃取剂与溶质不会发生反应.
解答 解:(1)CCl4从碘水中萃取碘并用分液漏斗分离两种溶液,操作为查漏→装液→振荡→静置→分液,则步骤为D→B→C→A→G→E→H→F,
故答案为:D;B;C;E;
(2)旋开活塞,分离下层液体,应使漏斗下端管口紧靠烧杯内壁,及时关闭活塞,不要让上层液体流出,(G)步骤目的为操作时漏斗里液体能够流出,
故答案为:使漏斗下端管口紧靠烧杯内壁,及时关闭活塞,不要让上层液体流出;使漏斗内外空气相通,以保证漏斗里的液体能顺利流出;
(3)四氯化碳是难溶于水的比水重的液体,密度比水大,分层后E中下层液体是溶解了碘单质的四氯化碳,溶液的颜色为紫红色,
故答案为:无;大;紫红;
(4)选用CCl4从碘水中萃取碘的原因是CCl4与水不互溶;而且碘在CCl4中的溶解度比在水中的大得多,
故答案为:CCl4与水不互溶;而且碘在CCl4中的溶解度比在水中的大得多.
点评 本题考查了分液的步骤和萃取剂的选择,选择萃取剂紧扣萃取剂的选择标准判断即可,要注意操作步骤的顺序和注意问题,题目难度中等.


 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
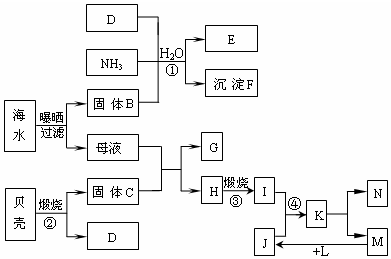
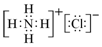 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.96% | B. | 5.66% | C. | 75% | D. | 12.5% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的处理具有重要意义.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 11.7g | B. | 23.4 g | C. | 35.1g | D. | 58.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2H2(g)+O2(g)═2H2O(1)△H=-571.6kJ/mol | B. | 2H2(g)+O2(g)═2H2O(1)△H=+571.6 kJ/mol | ||
| C. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-285.8 kJ/mol | D. | H2(g)+$\frac{1}{2}$O2(g)═H2O(1)△H=-285.8kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用水无法鉴别乙醇、甲苯和溴苯 | |
| B. | 可用酸性高锰酸钾溶液除去甲烷中的乙烯 | |
| C. | C2H5OOCCOOC2H5的名称:二乙酸乙二酯 | |
| D. | 除去苯中的苯酚可加入氢氧化钠溶液后分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 1.0 MPa | 2.0 MPa | 3.0 MPa | |
| 810℃ | 54.0% | a | b |
| 915℃ | c | 75.0% | d |
| 1000℃ | e | f | 83.0% |
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com