
已知中学化学中常见反应形式为:A+B=C+D+H2O,对于该反应叙述不正确的是
A.该反应可能是氧化还原反应 B.该反应可能是非氧化还原反应
C.C和D中至少有一种一定是盐类物质 D.A和B不一定是酸和碱
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源:2013届浙江省温州市龙湾中学高三第一次月考化学试卷(带解析) 题型:填空题
(14分)A—J是中学化学中常见的物质,它们之间的转化关系如下框图所示(部分产物已略去)。已知A是一种高熔点物质,J是一种红褐色沉淀。
请回答下列问题:
(1)A的化学式为 。
(2)H与I溶液混合后,发生反应的离子方程式是 。
G→J的化学方程式为 。
(3)D物质恰好溶于一定量的稀盐酸后,用合适的化学用语表示所得溶液显酸性原因 。
(4) 实验证明,硝酸发生氧化还原反应时,硝酸越稀对应还原产物中氮元素的化合价越低。某同学取一定量的C、E合金与一定量的很稀的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入一定浓度的氢氧化钠溶液,所加氢氧化钠的物质的量与产生的沉淀的物质的量(mol)的关系如左图所示。试回答下列问题:
①图中OC段没有沉淀生成,此阶段发生的离子方程式为:_______________________________。
②在DE段没有沉淀的物质的量没有变化,则此阶段发生反应的离子方程式为:_________________________________;
③B点对应的沉淀量为________________ mol,C点对应的横坐标为___________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
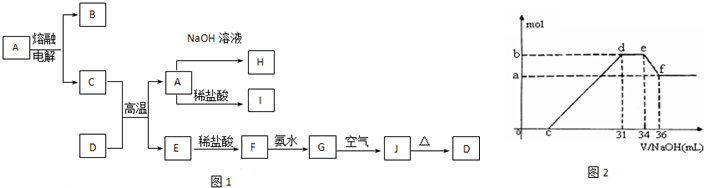
A—J是中学化学中常见的物质,它们之间的转化关系如下框图所示(部分产物已略去)。已知A是一种高熔点物质,J是一种红褐色沉淀。请回答下列问题:
 |
(1) A的化学式为
(2) H溶液中通入过量的CO2,其反应的离子方程式是
G→J的化学方程式为
(3) D物质恰好溶于一定量的稀盐酸后,用合适的化学用语表示所得溶液显酸性的原因
(4) 实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。某同学取一定量上述的C、E混合物 与一定量很稀的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入4mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。试回答下列问题:

① 图中o c段没有沉淀生成,此阶段发生反应的离子方程式为__________________________。
② 在d e段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式_______________ ;
上述现象说明溶液中_______结合OHˉ的能力最强(填离子符号)。
③ b与a的差值为_________mol。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年山东省枣庄三中高三(上)期末化学试卷(解析版) 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com