
·ÖĪö ·¢Éś·“Ó¦£ŗFe3O4+4CO=3Fe+4CO2£¬øł¾ŻøĒĖ¹¶ØĀɏ銓Äæ±źČČ»Æѧ·½³ĢŹ½£®
½ā“š ½ā£ŗŅŃÖŖ£ŗ¢ŁFe3O4£Øs£©+4C£ØŹÆÄ«£©?3Fe£Øs£©+4CO£Øg£©”÷H=+646.0kJ/mol£¬
¢ŚC£ØŹÆÄ«£©+CO2£Øg£©?2CO£Øg£©”÷H=+172.5kJ/mol£¬
øł¾ŻøĒĖ¹¶ØĀÉ£¬¢Ł-¢Ś”Į4æɵĆFe3O4£Øs£©+4CO£Øg£©=3Fe£Øs£©+4CO2£Øg£©£¬¹Ź”÷H=+646.0kJ/mol-4”Į£Ø+172.5kJ/mol£©=-44.0kJ/mol£¬¹Ź·“Ó¦ČČ»Æѧ·½³ĢŹ½ĪŖ£ŗFe3O4£Øs£©+4CO£Øg£©=3Fe£Øs£©+4CO2£Øg£©”÷H=-44.0kJ/mol£¬
¹Ź“š°øĪŖ£ŗFe3O4£Øs£©+4CO£Øg£©=3Fe£Øs£©+4CO2£Øg£©”÷H=-44.0kJ/mol£®
µćĘĄ ±¾Ģāæ¼²éČČ»Æѧ·½³ĢŹ½µÄŹéŠ“£¬ŌĖÓĆøĒĖ¹¶ØĀɽāĢāŹĒ¹Ų¼ü£¬ÄŃ¶Č²»“ó£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
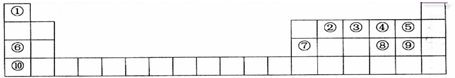
 £¬Ęä×īøßŃõ»ÆĪļĖ®»ÆĪļÓė¢ŽŗÅŌŖĖŲ×īøß¼ŪŃõ»ÆĪļĖ®»ÆĪļ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖAl£ØOH£©3+OH-=[Al£ØOH£©4]-_£®
£¬Ęä×īøßŃõ»ÆĪļĖ®»ÆĪļÓė¢ŽŗÅŌŖĖŲ×īøß¼ŪŃõ»ÆĪļĖ®»ÆĪļ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖAl£ØOH£©3+OH-=[Al£ØOH£©4]-_£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | øÖŗĶĢś | B£® | ½šøÕŹÆŗĶŹÆÄ« | C£® | ŗģĮ×ŗĶ°×Į× | D£® | ŃõĘųŗĶ³ōŃõ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·ÅµēŹ±£¬LiMn2O4·¢ÉśŃõ»Æ·“Ó¦£¬µē³ŲÄŚ²æLi+ĻņÕż¼«ŅĘ¶Æ | |
| B£® | ·ÅµēŹ±£¬Õż¼«·“Ó¦ĪŖ£ŗLi++LiMn2O4+e-ØTLi2Mn2O4 | |
| C£® | “×ĖįæÉÓĆ×÷ļ®Ąė×Óµē³ŲµÄµē½āÖŹ | |
| D£® | ³äµēŹ±£¬ļ®µÄĢ¼²ÄĮĻĪŖŃō¼«ĒŅ·“Ó¦ĪŖ£ŗLi++e-ØTLi |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | H2ŗĶD2 | B£® | O2ŗĶO3 | C£® | COŗĶCO2 | D£® | 12CŗĶ13C |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
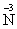 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | KOHµÄµē×ÓŹ½£ŗ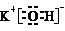 | |
| B£® | S2-µÄĄė×Ó½į¹¹Ź¾ŅāĶ¼£ŗ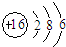 | |
| C£® | ŅŅČ²µÄ·Ö×ÓŹ½£ŗC2H4 | |
| D£® | ÖŹ×ÓŹżĪŖ6”¢ÖŠ×ÓŹżĪŖ8µÄĢ¼Ō×Ó£ŗ${\;}_{6}^{8}$C |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com