

| 编号 | ① | ② | ③ | ④ |
| 稀硝酸的体积/mL | 100 | 200 | 300 | 400 |
| 剩余金属的质量/g | 18.0 | 9.6 | 0 | 0 |
| NO 的体积/mL | 2240 | 4480 | 6720 | V |
分析 A、B、C、D是原子序数依次增大的四种短周期元素,B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同,核外电子排布为1s22s22p2,故B为碳元素;D原子有2个未成对电子,A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,M为HCHO,则A为H元素、D为O元素;C原子序数介于碳、氧之间,故C为N元素;E是第四周期元素,其原子核外最外层电子数与A原子相同,其余各层电子均充满,核外电子排布为1s22s22p63s23p63d104s1,则E为Cu.
(1)同周期随原子序数增大,第一电离能呈增大趋势,但原子处于全满、半满、全空时,能量较低,第一电离能高于同周期相邻元素;
(2)M为HCHO,根据分子中C原子σ键数目、孤电子对数确定杂化轨道数目,进而确定杂化方式;
(3)Cu失去4s能级1个电子形成Cu+;由晶胞结构可知,Cu+位于晶胞内部;
(4)分子之间存在氢键会使物质的熔沸点升高;
(5)CO2、N3-互为等电子体,二者结构相似,N3-中N原子之间形成2对共用电子对;
(6)负极发生氧化反应,由图可知,HCHO发生氧化反应生成二氧化碳,由守恒守恒可知还生成H+;
(7)由表中数据可知,实验①②都有金属剩余,硝酸完全反应,则溶液中不可能含有硝酸铁,溶液中金属离子为+2价,在实验①的基础上加入100mL硝酸,参加反应的金属的质量为18g-9.6g=8.4g,生成NO的体积为4480mL-2240mL=2240mL,NO物质的量为0.1mol,根据电子转移守恒可知,参加反应金属的物质的量为$\frac{0.1mol×(5-2)}{2}$=0.15mol,参加反应金属的平均摩尔质量为$\frac{8.4g}{0.15mol}$=56g/mol,故该过程只有Fe参加反应,故实验①只有Fe参与反应,发生反应为:3Fe+8HNO3═3Fe(NO3)2+2NO↑+4H2O,根据NO的体积结合方程式计算硝酸的物质的量,进而计算硝酸的物质的量浓度.
解答 解:A、B、C、D是原子序数依次增大的四种短周期元素,B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同,核外电子排布为1s22s22p2,故B为碳元素;D原子有2个未成对电子,A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,M为HCHO,则A为H元素、D为O元素;C原子序数介于碳、氧之间,故C为N元素;E是第四周期元素,其原子核外最外层电子数与A原子相同,其余各层电子均充满,核外电子排布为1s22s22p63s23p63d104s1,则E为Cu.
(1)同周期随原子序数增大,第一电离能呈增大趋势,但N原子2P能级为半满稳定状态,能量较低,第一电离能高于同周期相邻元素,故第一电离能:N>O>C,故答案为:N>O>C;
(2)M为HCHO,分子中C原子形成3个σ键、没有孤电子对,故杂化轨道数目为3,C原子采取sp2杂化方式,故答案为:sp2;
(3)Cu失去4s能级1个电子形成Cu+,基态核外电子排布式为1s22s22p63s23p63d10,由晶胞结构可知,Cu+位于晶胞内部,晶胞中含有4个Cu+,故答案为:1s22s22p63s23p63d10;4;
(4)NH3分子间能形成氢键,甲烷分子之间为分子间作用力,氢键比分子间作用力强,故NH3的沸点比CH4的高,故答案为:NH3分子间能形成氢键;
(5)CO2、N3-互为等电子体,二者结构相似,N3-中N原子之间形成2对共用电子对,N3-的结构式[N=N=N]-,故答案为:[N=N=N]-;
(6)负极发生氧化反应,由图可知,HCHO发生氧化反应生成二氧化碳,由守恒守恒可知还生成H+,负极所在的左室中发生反应的电极反应式是:HCHO-4e-+H2O=CO2+4H+,故答案为:HCHO-4e-+H2O=CO2+4H+;
(7)由表中数据可知,实验①②都有金属剩余,硝酸完全反应,则溶液中不可能含有硝酸铁,溶液中金属离子为+2价,在实验①的基础上加入100mL硝酸,参加反应的金属的质量为18g-9.6g=8.4g,生成NO的体积为4480mL-2240mL=2240mL,NO物质的量为0.1mol,根据电子转移守恒可知,参加反应金属的物质的量为$\frac{0.1mol×(5-2)}{2}$=0.15mol,参加反应金属的平均摩尔质量为$\frac{8.4g}{0.15mol}$=56g/mol,故该过程只有Fe参加反应,故实验①只有Fe参与反应,实验①发生反应为:3Fe+8HNO3═3Fe(NO3)2+2NO↑+4H2O,生成NO的物质的量为$\frac{2.24L}{22.4L/mol}$=0.1mol,根据方程式可知,参加反应的硝酸的物质的量为0.1mol×4=0.4mol,故硝酸的物质的量浓度为$\frac{0.4mol}{0.1L}$=4mol/L,故答案为:4.
点评 本题考查物质结构问题、混合物的有关计算、原电池原理等,(7)中根据表中数据判断各阶段发生的反应是解题关键,侧重对学生综合能力的考查,本题过程复杂、计算量较大,为易错题目,难度较大.


科目:高中化学 来源: 题型:解答题
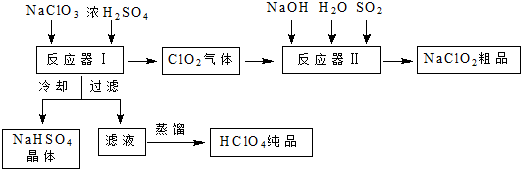
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
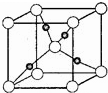 甲烷在一定条件下可生成以下微粒:
甲烷在一定条件下可生成以下微粒:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
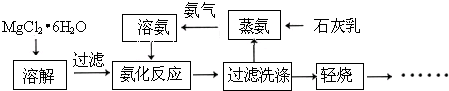
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ① | C. | ② | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | p=$\frac{17V+22400}{22.422.4V}$ | B. | W=$\frac{17c}{ρ}$ | ||
| C. | $\frac{17V}{17V+22400}$=W | D. | C=$\frac{1000Vρ}{17V+22400}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
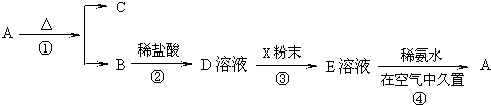
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com