
【题目】下列事实不能用勒夏特列原理来解释的是 ( )
A. 用排饱和食盐水的方法收集氯气
B. 合成氨工业选择高温(合成氨反应为放热反应)
C. 增大压强,有利于SO2和O2反应生成SO3
D. 在Fe3++3SCN-![]() Fe(SCN)3反应达平衡时,增加KSCN的浓度,体系颜色变深
Fe(SCN)3反应达平衡时,增加KSCN的浓度,体系颜色变深
科目:高中化学 来源: 题型:
【题目】反应2X(g)2Y(g)+2Z(g)△H>0达到平衡时,要使正反应速率降低,X的浓度增大,应采取的措施是( )
A.加压B.减压C.减小Z的浓度D.降温
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将pH均为3,体积均为V0的HA和HB溶液,分别加水稀释至体积V,pH随lg![]() 的变化如图所示,下列叙述正确的是
的变化如图所示,下列叙述正确的是
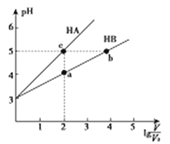
A. 水的电离程度:b>c>a
B. 若分别用等浓度的NaOH溶液完全中和,消耗NaOH的体积:b>a>c
C. 若分别用等浓度的NaOH溶液完全中和,所得溶液的pH:a>b>c
D. 溶液中离子总浓度: a>b>c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在容积为2L的密闭容器中发生反应CO(g)+H2O(g) ![]() CO2(g)+H2(g),部分数据见下表(表中t2>t1)
CO2(g)+H2(g),部分数据见下表(表中t2>t1)
反应时间/min | n(CO)/mol | n(H2O)/mol | n(CO2)/mol | n(H2)/mol |
0 | 1.20 | 0.60 | 0 | 0 |
t1 | 0.80 | |||
t2 | 0.20 |
下列说法正确的是
A. 反应在t1min末的速率为v(H2)=0.40/t1 mol·L-1·min-1
B. 平衡时CO的转化率为66.67%
C. 该温度下反应的平衡常数为1
D. 其他条件不变,若起始时,n(CO)=0.60 mol,n(H2O)=1.20 mol,则平衡时n(CO2)=0.20mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在3个体积相同的密闭容器中均发生下列反应:CO2(g)+H2(g) ![]() H2O(g)+CO(g),反应所处的温度相同,但起始浓度不同,其中甲:n(CO2)=amol,n(H2)=2amol;乙:n(CO2)=n(H2)=amol;丙:n(CO2)=n(H2)=n(CO) =amol.达到平衡时H2O(g)的物质的量由大到小的顺序是
H2O(g)+CO(g),反应所处的温度相同,但起始浓度不同,其中甲:n(CO2)=amol,n(H2)=2amol;乙:n(CO2)=n(H2)=amol;丙:n(CO2)=n(H2)=n(CO) =amol.达到平衡时H2O(g)的物质的量由大到小的顺序是
A. 甲>乙>丙 B. 甲>丙>乙 C. 乙>甲>丙 D. 乙>丙>甲
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既属于氧化还原反应,又属于吸热反应的是( )
A.Ba(OH)2·8H2O与NH4Cl的反应B.碳与二氧化碳的反应
C.铝片和稀盐酸反应D.甲烷在氧气中的燃烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在pH=1的溶液中能大量共存,并且溶液为无色透明的离子组是( )
A. Cu2+、SO42-、Cl-、Na+ B. OH-、K+、NO3-、Ba2+
C. Mg2+、SO42-、Al3+、Cl- D. Na+、HCO3-、K+、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1.76 g铜镁合金完全溶解于50 mL、密度为1. 40 g cm-3、质量分数为63%的浓硝酸中,得到NO2气体1 792 mL(标准状况),向反应后的溶液中加入适量的1.0 mol L-1的NaOH 溶液,恰使溶液中的金属离子全部沉淀。下列说法不正确的是
A. 该浓硝酸中的HNO3的物质的量浓度是14.0 mol L-1
B. 加入NaOH溶液的体积是50 mL
C. 浓硝酸在与合金的反应中起了酸性和氧化性的双重作用,且起氧化性的硝酸的物质的量为0.08 mol
D. 得到的金属氢氧化物的沉淀为3.12 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com