
| A. | 苯酚显酸性,是因为羟基对苯环影响的结果 | |
| B. | 分子式为C2H4和C3H6的物质一定互为同系物 | |
| C. | 聚合物  是苯酚和甲醛在一定条件下反应得到的高分子化合物 是苯酚和甲醛在一定条件下反应得到的高分子化合物 | |
| D. | 1mol 与足量的NaOH溶液加热充分反应,最多能消耗4mol NaOH 与足量的NaOH溶液加热充分反应,最多能消耗4mol NaOH |
分析 A.苯环影响酚-OH;
B.C3H6可能为烯烃或环丙烷;
C. 为酚醛树脂;
为酚醛树脂;
D.2个酚-OH、-个-COOC-及水解生成的酚-OH均与NaOH反应.
解答 解:A.苯酚显酸性,是因为苯环影响酚-OH,故A错误;
B.C3H6可能为烯烃或环丙烷,而C2H4为乙烯,不一定为同系物,故B错误;
C. 为酚醛树脂,为苯酚和甲醛在一定条件下反应得到的高分子化合物,故C正确;
为酚醛树脂,为苯酚和甲醛在一定条件下反应得到的高分子化合物,故C正确;
D.2个酚-OH、-个-COOC-及水解生成的酚-OH均与NaOH反应,则1mol与足量的NaOH溶液加热充分反应,最多能消耗4mol NaOH,故D正确;
故选CD.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物的官能团与性质、有机反应为解答的关键,侧重分析与应用能力的考查,注意有机物性质的应用,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:推断题
 、
、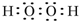 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 物质 | 丙酮 | 乙酸乙酯 | 乙醇 | 乙酸 |
| 沸点/℃ | 56.2 | 77.06 | 78 | 117.9 |
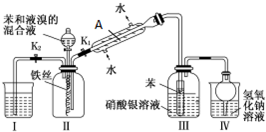
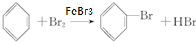
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu和浓硫酸在加热的条件下可以反应,体现浓硫酸的强氧化性和酸性 | |
| B. | 将SO2通入盛有品红溶液的试管中红色褪去,给试管加热无明显变化 | |
| C. | 将干燥的Cl2通入装有红色鲜花的试管中,红花褪色,说明Cl2具有漂白性 | |
| D. | 将蘸有浓氨水和浓硫酸的玻璃棒靠近,会产生白烟 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素X、Y的简单离子具有相同的电子层结构 | |
| B. | 由Z、W两种元素组成的化合物是离子化合物 | |
| C. | W的简单气态氢化物的热稳定性比X的强 | |
| D. | 离子半径:r(X)<r(Y)<r(Z)<r(W) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热稳定性:HF>H2O>NH3 | B. | 原子半径:F>O>N | ||
| C. | 沸点:乙烷>戊烷>丁烷 | D. | 酸性:H2SO4>H3PO4>HClO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 1:4 | C. | 4:1 | D. | 无法确定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com