
| A.SO2和O2 | B.NO和O2 | C.H2S和SO2 | D.NH3和HCl |
科目:高中化学 来源:不详 题型:单选题
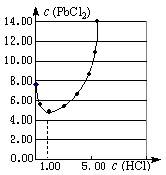
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①>② | B.①<② | C.①="②" | D.不能确定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 MnCl2+ Cl2↑+ 2H2O反应中,被氧化的HCl与参加反应的HCl质量关系是
MnCl2+ Cl2↑+ 2H2O反应中,被氧化的HCl与参加反应的HCl质量关系是| A.两者质量相等 |
| B.后者是前者的3倍 |
| C.前者是后者的1/2 |
| D.前者是后者的1/4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 )之比为6:1,则Cl2与NaOH溶液反应时,被氧化的氯气的体积分数为( )
)之比为6:1,则Cl2与NaOH溶液反应时,被氧化的氯气的体积分数为( )| A.0.25 | B.0.50 | C.0.75 | D.0.80 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
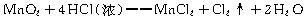
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
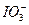 ,煮沸去掉过量的Br2;
,煮沸去掉过量的Br2;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com