
����Ŀ���赥�ʼ��仯����Ӧ�÷�Χ�ܹ㡣
(1)�Ʊ���뵼����ϱ����ȵõ��ߴ��裬��ҵ�Ͽ������²����Ʊ��ߴ��衣
��.��������̼��ԭ���������Ƶôֹ裻
��.�ֹ�������������450��500 �������·�Ӧ�Ƶ�SiCl4��
��.SiCl4Һ�徭�����ᴿ�������H2��1 100��1 200 �������·�Ӧ�Ƶøߴ��衣
��֪SiCl4�е�Ϊ57.6 �棬����H2Oǿ�ҷ�Ӧ��
��ش��������⣺
�ٵڢ�Ӧ�Ļ�ѧ����ʽΪ____________________________________��
�������Ʊ�����Ĺ����б����ϸ��������ˮ�����������¡�SiCl4�ڳ�ʪ�Ŀ�������ˮ���������ɫ����������������_______��H2��ԭSiCl4������������O2����������ĺ����________________________________________��
(2)�������豻��������������������ҵ����SiO2��Na2CO3��CaCO3��283 kg�ڸ�������ȫ��Ӧʱ�ų�CO2 44 kg���������IJ������û�ѧʽNa2SiO3��CaSiO3��xSiO2��ʾ��������x��________��
���𰸡� 2H2��SiCl4![]() Si��4HCl H2SiO3(��H4SiO4)��HCl ��ը 4
Si��4HCl H2SiO3(��H4SiO4)��HCl ��ը 4
��������(1)��������1 100��1 200 ���������������Ȼ��跴Ӧ���ɵ��ʹ���Ȼ��⣬�仯ѧ��Ӧ����ʽΪ��2H2��SiCl4![]() Si��4HCl����SiCl4�ڳ�ʪ�Ŀ�������ˮ���������ɫ��������SiCl4��ˮ��Ӧ����H2SiO3����H4SiO4����HCl��H2��ԭSiCl4������������O2����������ը����2�������Ļ�ѧ��ɿɸ��ݷ�Ӧԭ���õ���
Si��4HCl����SiCl4�ڳ�ʪ�Ŀ�������ˮ���������ɫ��������SiCl4��ˮ��Ӧ����H2SiO3����H4SiO4����HCl��H2��ԭSiCl4������������O2����������ը����2�������Ļ�ѧ��ɿɸ��ݷ�Ӧԭ���õ���
Na2CO3+SiO2![]() NaSiO3+CO2����CaCO3+SiO2
NaSiO3+CO2����CaCO3+SiO2![]() CaSiO3+CO2�����ɻ�ѧʽNa2SiO3CaSiO3xSiO2��Ӧ��Na2CO3��CaCO3�����ʵ�����ȣ�n��CO2��=n��Na2CO3��+n��CaCO3��=n��SiO2��Ӧ��=
CaSiO3+CO2�����ɻ�ѧʽNa2SiO3CaSiO3xSiO2��Ӧ��Na2CO3��CaCO3�����ʵ�����ȣ�n��CO2��=n��Na2CO3��+n��CaCO3��=n��SiO2��Ӧ��=![]() =1000mol��n��Na2CO3��=n��CaCO3��=500mol��500molNa2CO3��������53kg��500molCaCO3��������50kg��1000molSiO2��������60kg��n��SiO2������=
=1000mol��n��Na2CO3��=n��CaCO3��=500mol��500molNa2CO3��������53kg��500molCaCO3��������50kg��1000molSiO2��������60kg��n��SiO2������=![]() =2000mol����ʣ��Ķ�����������ɵĹ���ơ�������Ϊ2000��500��500=4��1��1������x=4����Ϊ��4��
=2000mol����ʣ��Ķ�����������ɵĹ���ơ�������Ϊ2000��500��500=4��1��1������x=4����Ϊ��4��


 ������ÿ�ʱ��ҵϵ�д�
������ÿ�ʱ��ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I.ijѧ��������ͼװ�òⶨ��Ӧ���������ų��������������к��ȡ���ش����⣺
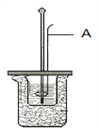
ͼ��A��������Ϊ__________���ձ���������ֽ����������____________��
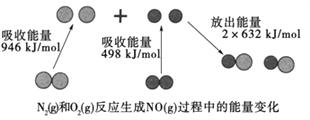
��.��ͼΪN2(g)��O2(g)��Ӧ����NO(g)�����е������仯ʾ��ͼ��
���ж�1mol N2(g)��1mol O2(g)���е�������__________2mol NO(g)���е����������������ڡ���С�ڡ���
��.������������Ӧ��A��2HCl+Ba(OH)2= BaCl2+2H2O��B��2Fe3++Cu= 2Fe2++Cu2+
��1����������Ӧ�ı��ʣ��ж�����Ƴ�ԭ��ص��ǣ�__________(�A����B�� )��
��2����������Ƴ�ԭ��صķ�Ӧѡ���ʺϵIJ��Ϻ��Լ����һ��ԭ��أ�
�ٸ���������_________���������Һ��__________��
��д�������ĵ缫��Ӧʽ______________��
��ԭ��ع���ʱ��Һ�е�Cl-��_________���ƶ����������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȼ�ϵ�أ�SOFC���Թ�����������Ϊ����ʣ��乤��ԭ����ͼ��ʾ�����й��ڹ���ȼ�ϵ�ص��й�˵������ȷ���ǣ�������
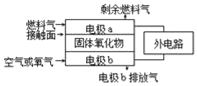
A. ������������������õ����ڵ����ͨ��
B. ������������O2����a����b���ƶ�
C. �缫bΪ��صĸ������缫��ӦʽΪ��O2+4e��=2O2��
D. ����C3H8Ϊȼ��������Ӵ����Ϸ����ķ�ӦΪC3H8��20e��+10O2���T3CO2+4H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��Ӧ�е������仯���ɻ�ѧ��Ӧ�оɻ�ѧ������ʱ���յ��������»�ѧ���γ�ʱ�ų���������ͬ����ģ���ͼΪN2��g����O2��g����Ӧ����NO��g�������е������仯������˵����ȷ����
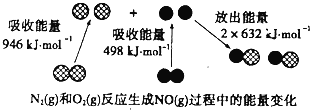
A. 1molN2��g����1molO2��g����Ӧ�ų�������Ϊ180kJ
B. ͨ������£�N2��g����O2�����ֱ������NO
C. NO��һ���������������NaOH��Һ��Ӧ�����κ�ˮ
D. 1molN2��g����1molO2��g�������������2molNO��g�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ��ϳ��������պ뾰�������ݾ���ע���м���ҩ��730�֣����С���ʯ����Ŀ��д������������ѩ������ǿ��֮�����������Գɻҡ���������ġ���ʯ����ָ�� ��
A.�Ȼ���
B.���ᰴ
C.�������
D.�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£���ӦN2O4(g) ![]() 2NO2(g)����H>0�����ܱ������дﵽƽ��.����˵������ȷ����
2NO2(g)����H>0�����ܱ������дﵽƽ��.����˵������ȷ����
A. ��ѹʱ(�����С)��ƽ�����淴Ӧ�����ƶ�����ʹ����Ӧ��������
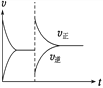
B. ijʱ�̸ı���������ʱ������ͼ���ı�������Ǻ���ʱ����N2O4��Ũ��
C. ����������䣬��������N2O4��ƽ��������Ӧ�����ƶ����ٴ�ƽ��ʱ��ɫ����
D. ����ѹǿ���䣬��������N2O4�������������ƽ��������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й����ʵ����ʻ���������ʵ�Ӧ�þ���ȷ���ǣ�������
A. ������Һ���������Һ�еĴ����������ˮ�⣬ͬŨ��ʱǰ�ߵ�ˮ��̶ȱȺ��ߵ�һЩ
B. ������ˮ������ˮ��ɱ���嶾ԭ����һ����
C. MgO��Al2O3�ڹ�ҵ�������������²��ϣ����õ�����������ұ��þ��������
D. �Ȼ�������Һ�������ɲ����յõ�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ִ���ʯ�ͻ���Ϊ����������ϳɲ����Ǣźϳɰ��������ϣ���ҽҩ���Ⱥϳ����ɺϳ����أ��ʺϳ���ά���˺ϳ�ϴ�Ӽ���
A. �ƢȢ� B. �ƢȢ� C. �ŢǢ� D. �Ȣɢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и����������ͬ���칹�����
A. ����������� B. ����������
C. ���������� D. 16O��18O
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com