
【题目】加热条件下,硅单质和HCl反应生成SiHCl3是粗硅提纯的重要步骤。某小组设计如图所示装置完成上述转化(夹持装置略去)。
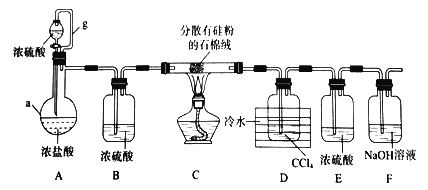
已知:SiHCl3的沸点为33.0°C,易溶于有机溶剂,能与水剧烈反应,在空气中易被氧化,CCl4的沸点为76.8°C。请回答:
(1)仪器a的名称为 ;导管g的作用为 ;
(2)装置A中,浓硫酸体现的性质为 ;实验时,需先打开分液漏斗活塞,一段时间后,在点燃C处酒精灯,理由是 ;
(3)装置C中发生反应的化学方程式为 ;
(4)装置D中所得的液态混合物的分离方法为 。(填操作名称)
(5)反应后的气体通过装置F中的NaOH溶液后,对逸出气体的处理方法为 ;
(6)SiHCl3在潮湿的空气中被氧化,生成一种氧化物和一种无氧酸,该反应的化学方程式为 。
【答案】(1)蒸馏烧瓶,平衡压强,使浓硫酸容易滴加;
(2)吸水性,排尽装置中的空气,避免SiHCl3与空气中的水蒸气反应和被O2氧化;
(3)Si+3HCl![]() SiHCl3+H2;(4)蒸馏;
SiHCl3+H2;(4)蒸馏;
(5)点燃;(6)2SiHCl3+O2+2H2O═2SiO2+6HCl。
【解析】
试题分析:(1)装置a带有支管,因此是蒸馏烧瓶,导管B的作用是平衡压强,使浓硫酸容易滴加;(2)浓硫酸遇水放出大量的热,使氯化氢挥发,因此利用浓硫酸的吸水性,SiHCl3在空气中容易被氧化,因此先通一段时间的氯化氢,排除装置中的空气,避免与氧气发生反应;(3)装置C是制备SiHCl3,因此根据投入物质,发生的反应是Si+3HCl![]() SiHCl3+H2;(4)根据SiHCl3易溶于有机溶剂,装置D中液体是SiHCl3的四氯化碳溶液,因此采用蒸馏的方法进行分离;(5)根据装置C中发生的反应,产生氢气,氢气是可燃性气体,通过点燃的方法除去;(6)在潮湿的空气中,说明有水参加反应,被氧化,说明氧气参加反应,生成一种氧化物,此氧化物是SiO2,无氧酸是HCl,因此化学反应方程式为2SiHCl3+O2+2H2O═2SiO2+6HCl。
SiHCl3+H2;(4)根据SiHCl3易溶于有机溶剂,装置D中液体是SiHCl3的四氯化碳溶液,因此采用蒸馏的方法进行分离;(5)根据装置C中发生的反应,产生氢气,氢气是可燃性气体,通过点燃的方法除去;(6)在潮湿的空气中,说明有水参加反应,被氧化,说明氧气参加反应,生成一种氧化物,此氧化物是SiO2,无氧酸是HCl,因此化学反应方程式为2SiHCl3+O2+2H2O═2SiO2+6HCl。


科目:高中化学 来源: 题型:
【题目】氮、磷及其化合物在生产、生活中有重要的用途。回答下列问题:
(1)在碱性条件下,次磷酸盐可用于化学镀银,完成其反应的离子方程式:
口H2PO2-+口Ag++口________=口PO43-+口Ag+口________
(2)由工业白磷(含少量砷、铁、镁等)制备高纯白磷(熔点44℃,沸点280℃),主要生产流程如下:
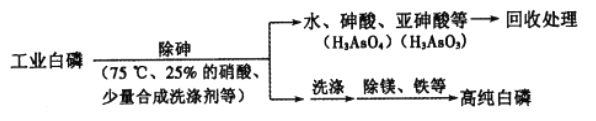
①关于除砷条件的说法合理的是__________(填字母)。
a.75℃使白磷熔化,并溶于水 b.硝酸浓度不易过大,防止白磷反应
c.温度不易过高,防止硝酸分解 d.适当提高温度,加快化学反应速率
②硝酸氧化除砷时被还原为NO,氧化相同质量的砷.当转化为亚砷酸的量越多,消耗硝酸的量越 _____________(填“多”或“少”)。
③某条件下,用一定量的硝酸处理一定量的工业白磷,砷的脱除率及磷的产率随硝酸质量分数的变化如右图,砷的脱除率从a点到b点降低的原因是_____________。

(3)某温度下,已知:
Ag+(aq)+2NH3(aq) ![]() Ag(NH3)2+(aq) k1=1.10×107
Ag(NH3)2+(aq) k1=1.10×107
AgCl(s)![]() Ag+(aq)+Cl-(aq) K2=1.45×10-10
Ag+(aq)+Cl-(aq) K2=1.45×10-10
①反应平衡常数的表达式K1=______________。
②计算可逆反应AgCl(s)+2NH3(aq)![]() Ag(NH3)2+(aq)+Cl-(aq)的化学平衡常数K=___________(保留2位有效数字)。
Ag(NH3)2+(aq)+Cl-(aq)的化学平衡常数K=___________(保留2位有效数字)。
③1Llmol/L氨水中最多可以溶解AgCl__________mol(保留1位有效数字,忽略溶液体积变化)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化中,一定要加入适当的还原剂才能实现的是( )
A.KMnO4→MnO2 B.HCl→Cl2
C.Fe2O3→Fe D.CaO→CaCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《奔跑吧兄弟》是一档热播的娱乐节目,其中蕴含着许多化学知识,其中一期节目,队员用水枪将酚酞溶液喷射到对方的“名牌”上,立即变红色。事先浸泡“名牌”的溶液可能是()
A.白酒 B.纯碱溶液 C.食盐溶液 D.柠檬酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用密度为1.25 g mL-1、质量分数为36.5%的浓盐酸配制240 mL 0.1 mol L-1的盐酸,请回答下列问题:
(1)浓盐酸的物质的量浓度为 。
(2)配制 240 mL 0.1 mol L-1的盐酸
应量取浓盐酸体积/mL | 应选用容量瓶的规格/mL |
(1)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次) 。
A.用30 mL水洗涤烧杯内壁和玻璃棒23次,洗涤液均注入容量瓶,振荡
B.用量筒淮确量取所需的浓盐酸的体积,倒入烧杯中,再加入少量水(约30 mL), 用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线12 cm处
(4)若实验中遇到下列情况,对盐酸溶液的物质的量浓度有何影响(填“偏高”、“偏低”或“不变”)?
①用于稀释盐酸的烧杯未洗涤, 。
②容量瓶中原有少量蒸馏水, 。
③定容时观察液面俯视, 。
(5)若实验过程中出现如下情况如何处理?
①定容时加蒸馏水时超过了刻度 。
②向容量瓶中转移溶液时有滚液不慎有溶液溅出 。
③定容摇勻后发现液面下降 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同体积,相同pH的某一元强酸溶液①和某一元弱酸溶液②分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是( )
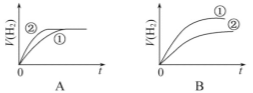
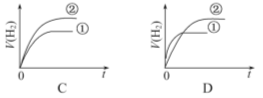
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列反应中,水既不是氧化剂,也不是还原剂的是
A.2Na+2H20=2Na0H+H2↑ B.C12+H20=HC1+HC10
C.2F2+2H20=4HF+02 D.2H20![]() 2H2↑+02↑
2H2↑+02↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中氯离子浓度与50mL1mol·L-1的AlCl3溶液中氯离子浓度相等的是 ( )
A.150mL1mol·L-1的NaCl B.150mL3mol·L-1的KCl
C.75mL2 mol·L-1的CaCl2 D.75mL2mol·L-1的NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一支25 mL的酸式滴定管中加入0.1 mol/L的HCl溶液,其液面恰好在5 mL刻度处,若把滴定管中的溶液全部放入烧杯中,然后用0.1 mol/L的NaOH溶液进行中和,则所需NaOH溶液的体积( )
A. 等于5 mL B. 大于20 mL C. 等于20 mL D. 小于20 mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com