
| A. | 把绿豆大的钾投入水中 | |
| B. | 把除去氧化膜的镁带放入少量冷水中 | |
| C. | 把溴水滴加到KI溶液中,并加入少量四氯化碳溶液 | |
| D. | 把铜片和铁片紧靠在一起浸入稀硫酸中 |
分析 A.钾性质活泼,与水剧烈反应;
B.镁与冷水不反应;
C.溴单质氧化碘离子为单质碘,易溶于四氯化碳呈紫色;
D.把铜片和铁片紧靠在一起浸入稀硫酸中,该装置构成了原电池,铜作正极;
解答 解:A.钾性质活泼,与水剧烈反应,放出大量的热并有气泡生成,现象明显且剧烈,故A不选;
B.镁与冷水不反应,可与热水发生反应,把一段打磨过的镁带放入少量冷水中,不能观察到明显变化,故B选;
C.Br2+2KI=2KBr+I2,静止分层,上层液体呈无色下层液体呈紫色,故C不选;
D.把铜片和铁片紧靠在一起浸入稀硫酸中,该装置构成了原电池,铁作负极,铜作正极,电子从铁片沿导线流向铜片,所以氢离子在铜片表面得电子生成氢气,故D不选.
故选B.
点评 本题考查元素化合物的性质、原电池原理、氧化还原反应和反应现象的掌握,题目难度不大,注意常见元素化合物的性质.


科目:高中化学 来源: 题型:选择题
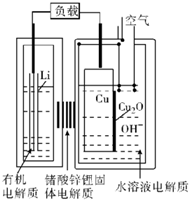 近年来AIST报告正在研究一种“高容量、低成本”锂-铜空气燃料电池.该电池放电时的反应过程为2Li+Cu2O+H2O=2Cu+2Li++2OH-,下列说法不正确的是( )
近年来AIST报告正在研究一种“高容量、低成本”锂-铜空气燃料电池.该电池放电时的反应过程为2Li+Cu2O+H2O=2Cu+2Li++2OH-,下列说法不正确的是( )| A. | 放电时,Li+透过固体电解质向Cu极移动 | |
| B. | 放电时,Cu作电池的负极 | |
| C. | 通空气时,铜被氧化,表面产生Cu2O | |
| D. | 整个反应过程中,铜相当于催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯酚、酒精、福尔马林均可用于消毒杀菌 | |
| B. | 硝基苯转化成苯胺(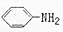 )的过程属于氧化反应 )的过程属于氧化反应 | |
| C. | 甲苯与浓硝酸、浓硫酸的混合酸反应可以获得邻、对位硝基甲苯 | |
| D. | 用食醋可除去热水壶内壁的水垢 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
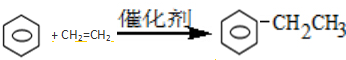 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化碳分子的结构式为 O-C-O | |
| B. | 氟化钠的电子式: | |
| C. | F原子的结构示意图: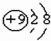 | |
| D. | 用电子式表示氯化氢分子的形成过程: |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
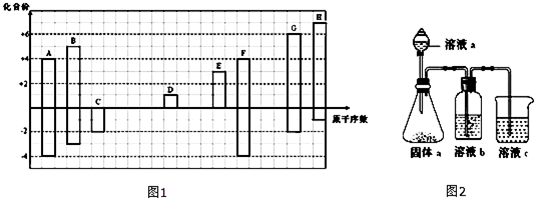
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
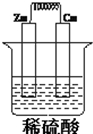 如图所示,将锌,铜通过导线相连,置于稀硫酸中构成原电池,完成下空
如图所示,将锌,铜通过导线相连,置于稀硫酸中构成原电池,完成下空查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 周期/族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | 0 |
| 2 | ④ | ⑤ | ⑥ | ⑨ | ||||
| 3 | ① | ② | ③ | ⑦ | ⑧ |
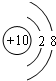 .
.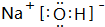 (填电子式),其所含有的化学键类型有离子键、极性共价键(请选择“离子键”、“极性共价键”、“非极性共价键”中的一个或几个填写).
(填电子式),其所含有的化学键类型有离子键、极性共价键(请选择“离子键”、“极性共价键”、“非极性共价键”中的一个或几个填写).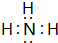 ,其水溶液呈碱性(填“酸性”、“中性”或“碱性”).
,其水溶液呈碱性(填“酸性”、“中性”或“碱性”).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com