
室温下,在pH=12的某溶液中,分别有甲、乙、丙、丁四位同学计算出由水电离出的[OH-]的数据分别为甲:1.0×10-7 mol· L-1;乙:1.0×
L-1;乙:1.0×
10-6 mol·L-1;丙:1.0×10-2 mol·L-1;丁:1.0×10-12 mol·L-1。其中你认为可能正确的数据是( )
A.甲、乙 B.乙、丙 C.丙、丁 D.乙、丁
科目:高中化学 来源: 题型:
将2 mol X和2 mol Y充入2 L的密闭容器中发生如下反应:X(g)+3Y(g)  2Z(g)+aQ(g),2 min达到平衡时生成0.8 mol Z,测得Q的浓度为
2Z(g)+aQ(g),2 min达到平衡时生成0.8 mol Z,测得Q的浓度为
0.4 mol·L-1,下列叙述错误的是( )
A.a的值为2
B.平衡时X的浓度为0.2  mol·L-1
mol·L-1
C.Y的转化率为60%
D.反应速率v(Y)=0.3 mol·(L·min)-1
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)二氧化硫的催化氧化的过程如图所示:
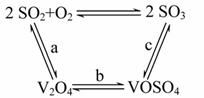
其中a、c二步的化学方程式可表示为____________
SO2+V2O5 SO3+V2O4
SO3+V2O4
4VOSO4+O2 2V2O5+4SO3
2V2O5+4SO3
该反应的催化剂是__________(写化学式)。
(2)550 ℃时,SO2转化为SO3的平衡转化率(α)与体系总压强(p)的关 系如图所示:
系如图所示:
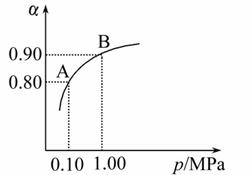
将2.0 mol SO2和1.0 mol O2置于5 L密闭容器中,反应达平衡后,体系总压强为0.10 MPa。试计算反应2SO3 2SO2+O2 在550 ℃时的平衡常数K=_________。
2SO2+O2 在550 ℃时的平衡常数K=_________。
(3)550 ℃时,将2.0 mol SO2和1.0 mol O2置于5 L密闭容器中,反应达平衡后,下列措施中能使n(SO3)/n(SO2)增大的是_____________。
A.升高温度
B.充入He(g),使体系总压强增大
C.再充入2.0 mol SO2和1.0 mol O2
(4)维持温度不变条件下使之发生如下反应:
2SO2+O2 2SO3,有两只密闭容器A和B。A容器有一个可以移动的活塞能使容器内保持恒压,B容器能保持恒容。起始时向这两个容器中分别充入等物质的量的体积比为2∶1的SO2和O2的混合气体,并使A和B容积相等,如图所示:
2SO3,有两只密闭容器A和B。A容器有一个可以移动的活塞能使容器内保持恒压,B容器能保持恒容。起始时向这两个容器中分别充入等物质的量的体积比为2∶1的SO2和O2的混合气体,并使A和B容积相等,如图所示:

试填写下列空格:
A容器达到平衡时所需的时间比B容器___________(填“短”或“长”);平衡时A容器中SO2的转化率 比B容器_________(填“大”或“小”);达到所述平衡后,若向两容器中通入等物质的量的原反应气体,达到平衡时,A容器的混合气体中SO3的体积分数__________(填“增大”“减小”或“不变”,下同);B容器的混合气体中SO3的体积分数__________。
比B容器_________(填“大”或“小”);达到所述平衡后,若向两容器中通入等物质的量的原反应气体,达到平衡时,A容器的混合气体中SO3的体积分数__________(填“增大”“减小”或“不变”,下同);B容器的混合气体中SO3的体积分数__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在0.1 mol·L-1 NaHCO3溶液中有关微粒浓度的关系正确的是( )
A.[Na+]+[H+]=[HCO3-]+[CO32-]+[OH-]
B.[Na+]=[HCO3-]+[CO32-]+[H2CO3]
C.[Na+]>[HCO3-]>[CO32-]>[H+]>[OH-]
D.[OH-]=[H+]+[H2CO3]+[HCO3-]
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)现有0.1 mol·L-1的纯碱溶液,试用pH试纸测定溶液的pH,其正确的操作是_______________________________________________________;
纯碱溶液呈碱性的原因是(用离子方程式表示)___________________________。
(2)为探究纯碱溶液呈碱性是由CO32-引起的,请你设计一个简单的实验方案:
__________________________________________________________________。
(3)为证明盐的水解是吸热反应,四位学生分别设计了如下方案,其中正确的是
_____________。
A.甲学生:在醋酸钠溶液中滴入2滴酚酞溶液,加热后红色加深,说明盐类水解是吸热反应
B.乙学生:在盐酸中加入氨水,混合液温度上升,说明盐类水解是吸热反应
C.丙学生:将硝酸铵晶体溶于水,水温下降,说明盐类水解是吸热反应
D.丁学生:在氨水中加入氯化铵固体,溶液的pH变小,说明盐类水解是吸热反应
B项中和反应本身是放热反应,C项是因为NH4NO3溶于水吸热,D项是因为NH4Cl抑制NH3·H2O 的电离而使pH变小
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是元素周期表的一部分,有关说法不正确的是( )
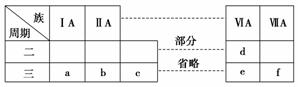
A.元素e的氧化物对应的水化物均为强酸
B.a、b、d、e四种元素的离子半径:e>d>a>b
C.b、f两种元素形成的化合物为离子化合物
D.a、c、e的最高价氧化物对应的水化物之间能够相互反应
查看答案和解析>>
科目:高中化学 来源: 题型:
LiH可作飞船的燃料,已知下列反应:
①2Li(s)+H2(g)===2LiH(s) ΔH=-182 kJ·mol-1;
②2H2(g)+O2(g)===2H2O(l) ΔH=-572 kJ·mol-1;
③4Li(s)+O2(g)===2Li2O(s) ΔH=-1 196 kJ·mol-1。
则LiH在O2中燃烧的热化学方程式为( )
A.2LiH(s)+O2(g)===Li2O(s)+H2O(l) ΔH=-702 kJ·mol-1
B.2LiH(s)+O2(g)===Li2O(s)+H2O(l) ΔH=-1 950 kJ·mol-1
C.2LiH(s)+O2(g)===Li2O(s)+H2O(l) ΔH=-1 586 kJ·mol-1
D.2LiH(s)+O2(g)===Li2O(s)+H2O(g) ΔH=-988 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系:甲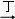 乙
乙 丙.下列有关物质的推断不正确的是( )
丙.下列有关物质的推断不正确的是( )
|
| A. | 若甲为焦炭,则丁可能是O2 |
|
| B. | 若甲为Fe,则丁可能是Cl2 |
|
| C. | 甲不可能是Mg |
|
| D. | 若甲为Ca(OH)2溶液,则丁可能是CO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com