
| A. | c=$\frac{1000ρ×a%}{M}$×2 | B. | a=$\frac{cMV}{1000}$ | C. | c=$\frac{CM}{200ρ}$ | D. | V×ρ×a%=$\frac{cMV}{1000}$ |
分析 A.先根据c=$\frac{1000ρω}{M}$计算c(X2CO3),然后根据c=2c(X2CO3)计算;
B.根据溶解度s=$\frac{{m}_{溶质}}{{m}_{溶剂}}$×100g计算;
C.根据c(c(X2CO3)=$\frac{1000ρω}{M}$计算c(X2CO3),然后根据c=2c(X2CO3)计算溶质的质量分数为a%;
D.V×ρ×a%表示溶质X2CO3 的质量,根据m=cVM计算出X2CO3 的质量,根据计算结果进行判断.
解答 解:A.c(X2CO3)=$\frac{1000ρω}{M}$=$\frac{1000ρ×a%}{M}$,则c=c(X+)=2c(X2CO3)=$\frac{1000ρ×a%}{M}$×2,故A正确;
B.溶液中m(X2CO3)=nM=$\frac{1}{2}$×cV×$\frac{1}{1000}$×M=$\frac{cVM}{2000}$g,溶液的质量为ρV,则溶解度s=$\frac{{m}_{溶质}}{{m}_{溶剂}}$×100g=$\frac{\frac{cVM}{2000}}{ρV-\frac{cVM}{2000}}$×100g=$\frac{100cM}{2000ρ-cM}$g,故B错误;
C.c(R2CO3)=$\frac{1}{2}$c(X+)=0.5cmol•L-1,m(X2CO3)=0.5cmol•L-1×Mg/mol=0.5cMg=ρV×a%,整理可得:a=$\frac{50cM}{ρV}$,故C错误;
D.V×ρ×a%表示溶质R2CO3 的质量,溶液中m(X2CO3)=nM=$\frac{1}{2}$×$\frac{mcV}{1000}$,二者质量不相等,故D错误,
故选A.
点评 本题考查溶液浓度有关计算,涉及物质的量浓度、质量分数、溶解度等,注意掌握物质的量浓度与质量分数之间的关系,题目属于字母型计算,增大计算难度,为易错题目,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 1 mol乙烷在光照条件下最多能与3 mol Cl2发生取代反应 | |
| B. | 石油裂解气能使溴的四氯化碳溶液、酸性KMnO4溶液褪色 | |
| C. | 水煤气可用来合成液态烃、甲醇等有机物 | |
| D. | 苯可通过取代反应制得硝基苯、氯苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
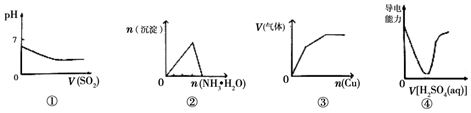
| A. | 图①表示将二氧化硫通入到一定量氯水中 | |
| B. | 图②表示将氨水滴入到一定量氯化铝溶液中 | |
| C. | 图③表示将过量铜粉加入到一定量浓硝酸中 | |
| D. | 图④表示将稀硫酸滴加到Ba(OH)2溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某反应中存在Na+、ClO-、Cl-、CN-、HCO3-、N2、H2O七种微粒,反应过程中测得ClO-和N2的物质的量随时间变化的曲线如图所示.下列判断正确的是( )
某反应中存在Na+、ClO-、Cl-、CN-、HCO3-、N2、H2O七种微粒,反应过程中测得ClO-和N2的物质的量随时间变化的曲线如图所示.下列判断正确的是( )| A. | 还原剂是含CN-的物质,氧化产物只有N2 | |
| B. | 氧化剂是ClO-,还原产物是HCO3- | |
| C. | 配平后还原剂与氧化剂的化学计量数之比为2:5 | |
| D. | 若生成2.24L(标准状况)N2,则反应中转移电子0.2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子总数为NA的NO2和CO2混合气体含有的氧原子数为2NA | |
| B. | 含有NA个原子的氢气在标准状况下的体积约为11.2 L | |
| C. | 常温常压下,92 g的NO2和N2O4混合气体含有的原子数为6NA | |
| D. | 40 g NaOH溶解在1 L水中,所制得的100 mL溶液中含Na+数为0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸钡难溶于水,在水溶液中不能导电,所以硫酸钡不是电解质 | |
| B. | 电解质的电离一定要在水分子作用下才能进行 | |
| C. | 三氧化硫溶于水能导电,所以三氧化硫是电解质 | |
| D. | 硫酸、氢氧化钡、纯碱、苛性钠都是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
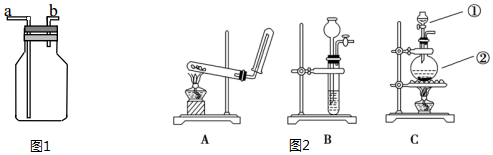
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯乙烯的结构式:H2C=CHCl | B. | S2-的结构示意图: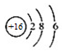 | ||
| C. | 熟石膏的化学式:2CaSO4•H2O | D. | 二氧化碳的比例模型: |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com