
【题目】纳米碳酸钙是一种广泛应用于塑料、食品、医药、饲料等行业的重要无机填料。以磷石膏钙渣为原料制取高品质纳米碳酸钙的工艺流程如下:

已知某磷石膏钙渣的主要成分及其含量如下表所示。
CaO | P2O5 | SO3 | Fe2O3 | Al2O3 | SiO2 | 烧失量 |
47.70% | 1.60% | 1.77% | 0.041% | 0.0027% | 9.85% | 37.69% |
请回答下列问题:
(1)对磷石膏钙渣进行酸溶的目的是获得机制CaCl2溶液,为了提高溶出率,可以采取的措施有______。(回答两条即可)
(2)为了探究酸溶的工艺条件,称取6 份各50g磷石膏钙渣,分别用不同浓度盐酸进行溶解,反应时间为30 min,测得滤液中钙溶出率的结果如图所示,最适宜的盐酸浓度为_______。

(3)精制是向粗制CaCl2溶液中通入氨气,控制溶液的pH,主要除去________ (填金属阳离子)。
(4)碳化时,先将精制CaCl2溶液稀释至一定体积,控制反应温度以及NH3和CO2 的通入量,此过程中,通入气体有先后顺序,应先通入气体的化学式_______(填化学式);碳化时发生反应的化学方程式为______。
(5)把CaCO3浊液滴入1.0molL-1 的Na2SO3溶液中,能否产生CaSO3沉淀?_______。若不能,说明原因;若能,请从定量的角度简述判断依据:_______。[已知:Ksp(CaSO3)=1.4×10-7,Ksp(CaCO3)=2.8×10-9]
(6)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级:__________。
【答案】 粉碎磷石膏钙渣,增大盐酸浓度,适当升高温度,延长酸溶时间等(任写两条) 4.0 molL-1(填4.0mol/L左右均可) Fe3+、Al3+ NH3 CaCl2+H2O+2NH3+CO2=CaCO3↓+2NH4Cl 能 由![]() =50 可知,当CaSO3与CaCO3 的混合液中c(SO32-)>50c(CO32-)时,即发生由CaCO3向CaSO3的转变 略
=50 可知,当CaSO3与CaCO3 的混合液中c(SO32-)>50c(CO32-)时,即发生由CaCO3向CaSO3的转变 略
【解析】(1)磷石膏钙渣进行酸溶时,为了提高溶出率,可以采取粉碎磷石膏钙渣,增大盐酸浓度,适当升高温度,延长酸溶时间等方法;正确答案:粉碎磷石膏钙渣,增大盐酸浓度,适当升高温度,延长酸溶时间等(任写两条)。
(2)根据图像可知,盐酸的浓度控制在4.0mol·L-1时或左右,钙溶出率较高;正确答案:4.0mol·L-1(填4.0mol·L-1左右均可)
(3)磷石膏钙渣进行酸溶时,溶液中存在铁离子、铝离子等杂质离子,因此,向粗制CaCl2溶液中通入氨气,控制溶液的pH,把Fe3+、Al3+变为沉淀而除去;正确答案:Fe3+、Al3+。
(4)二氧化碳易与含有氨气的碱性CaCl2溶液反应,有利于反应的顺利进行,生成碳酸钙沉淀和氯化铵,反应为:CaCl2+H2O+2NH3+CO2=CaCO3↓+2NH4Cl,因此先通入气体为NH3;正确答案:NH3 ; CaCl2+H2O+2NH3+CO2=CaCO3↓+2NH4Cl。
(5)由![]() =c(Ca2+)×c(SO32-)/c(Ca2+)×c(CO32-)=c(SO32-)/c(CO32-)=1.4×10-7/2.8×10-9=50,c(SO32-)/c(CO32-)=50, 当CaSO3与CaCO3的混合液中c(SO32-)>50c(CO32-)时,即发生由CaCO3向CaSO3的转变; 正确答案:能;由
=c(Ca2+)×c(SO32-)/c(Ca2+)×c(CO32-)=c(SO32-)/c(CO32-)=1.4×10-7/2.8×10-9=50,c(SO32-)/c(CO32-)=50, 当CaSO3与CaCO3的混合液中c(SO32-)>50c(CO32-)时,即发生由CaCO3向CaSO3的转变; 正确答案:能;由![]() =50可知,当CaSO3与CaCO3的混合液中c(SO32-)>50c(CO32-)时,即发生由CaCO3向CaSO3的转变。
=50可知,当CaSO3与CaCO3的混合液中c(SO32-)>50c(CO32-)时,即发生由CaCO3向CaSO3的转变。
(6)碳酸钙样品颗粒为纳米级时,其水溶液为胶体,可以用丁达尔效应进行检验;具体操作:取少量样品和水混合形成分散系,用一束光照射,若出现一条光亮的通路,则是纳米级,否则不是;正确答案:取少量样品和水混合形成分散系,用一束光照射,若出现一条光亮的通路,则是纳米级,否则不是。


科目:高中化学 来源: 题型:
【题目】在密闭容器中A与B反应生成C,其反应速率分别用v(A),v(B),v(C)表示,已知v(A),v(B),v(C)之间有以下关系3v(A)=2v(B),3v(C)=2v(B),则此反应可表示为( )
A.2A+3B=2C
B.A+3B=2C
C.3A+B=2C
D.A+B=C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】AgNO3是中学化学常用试剂,某兴趣小组设计如下实验探究其性质。
I. AgNO3的热稳定性
AgNO3受热易分解,用下图装置加热AgNO3固体,试管内有红棕色气体生成,一段时间后,在末端导管口可收集到无色气体a。

(1)实验室检验气体a的方法为_______________________________________。
(2)已知B中只生成一一种盐,据此判断AgNO3受热分解的化学方程式为______________。
(3)从安全角度考虑,上述实验装置存在一处明显缺陷,改进措施为______________________。II. AgNO3与盐溶液的反应

(4)甲同学认为试管②中产生银镜是Fe2+所致,其离子方程式为_____________________;
乙同学认为要判断该观点正确,需增加如下实验,取2 mL0.5mol/L AgNO3溶液于试营中,向其中满加几滴____________,若只产生白色远淀,证明甲同学观点正确。
(5)已知:AgSCN为白色沉淀。试管③中红色褪去的原因为__________________________(请从平衡移动的角度解释)。
(6)设计实验证明Ksp(AgI)sp(AgSCN)。
限选试剂:0.1 mol/L AgNO3溶液、0.1mol/LKI溶液、0.1mol/LKSCN 溶液___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外兴趣小组用下图装置探究条件对Na2S2O3溶液与稀H2SO4反应速率的影响。请回答有关问题。
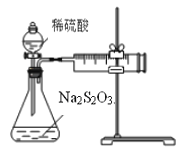
(1)写出该反应的离子方程式_______________________________________________________。
(2)连接好仪器后,开始实验前还需进行的操作是_____________________________________。
(3)现探究浓度对该反应速率(单位mL/min)的影响。
①应测定的实验数据为_____________。
②该实验实施过程中测定的气体体积比实际值偏小的一个重要原因是:____________________。
(4)若该小组同学设计了如下四组实验,
实验 | 反应温度 /℃ | Na2S2O3溶液 | 稀H2SO4 | H2O | |||
V/mL | c/(mol/L) | V/mL | c/(mol/L) | V/mL | |||
A | 25 | 5 | 0.1 | 10 | 0.1 | 5 | |
B | 25 | 5 | 0.2 | 5 | 0.2 | 10 | |
C | 35 | 5 | 0.1 | 10 | 0.1 | 5 | |
D | 35 | 5 | 0.2 | 5 | 0.2 | 10 | |
① 实验数据体现了反应物__________(填化学式)的浓度及__________条件对反应速率的影响。
② 预测反应速率最快的一组实验序号为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、Q是四种短周期元素,X元素M层上的电子数是原子核外电子层数的2倍;Y原子最外层电子数是次外层电子数的2倍;Z元素的单质为双原子分子,Z的氢化物水溶液呈碱性;W元素最高正价与最低负价之和为6;Q是地壳中含量最高的金属元素。
回答下列问题:
(1)X元素在元素周期表中的位置_______________________________________。
(2)由Y和W形成的化合物的电子式________。
(3)YX2分子的结构式为________,其化学键类型为是_________。
(4)前四种元素的简单氢化物中Z的沸点最高,原因是________________________________。
(5)写出Q和W两种元素的最高价氧化物的水化物发生反应的离子方程式___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中加入A、B、C三种气体,保持一定温度,在t1~t4时刻测得各物质的浓度如下表。据此判断下列结论正确的是( )
测定时刻/s | t1 | t2 | t3 | t4 |
c(A)/(mol/L) | 6 | 3 | 2 | 2 |
c(B)/(mol/L) | 5 | 3.5 | 3 | 3 |
c(C)/(mol/L) | 1 | 2.5 | 3 | 3 |
A.在t3时刻反应已经停止
B.A的转化率比B的转化率低
C.在容器中发生的反应为:2A+B![]() 2C
2C
D.在t2~t3内A的平均反应速率为:[1/(t3-t2)]mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2和H2合成NH3的能量变化如图所示,该反应的热化学方程式是( )

A. N2(g)+3H2(g) = 2NH3(g) ;△H = 2(b—a) kJ/mol
B. N2(g)+3H2(g) = 2NH3(l); △H = 2(a—b—c) kJ/mol
C. N2(g)+3H2(g) = 2NH3(l) ;△H = (b+c—a) kJ/mol
D. N2(g)+3H2(g) = 2NH3(g) ;△H = (a+b) kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜 - 锌原电池如图所示,电解质溶液为硫酸铜溶液,电池工作一段时间后,下列说法错误的是
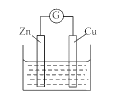
A. 锌电极上的反应为Zn- 2e-=Zn2+
B. 溶液中的SO42-向锌电极移动
C. 电子从锌电极经过硫酸铜溶液流向铜电极
D. 铜电极质量增加
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关数据的比较,不正确的是( )
A. 元素的价电子数和所在族的族序数相等
B. NaOH晶体中的阳离子和阴离子数目相等
C. CsCl晶体中每个Cs+周围紧邻的Cl-和每个Cl-周围紧邻的Cs+个数相等
D. [Co(NH3)6]3+中的NH3分子数与配位键数相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com