
| A. | H+、SO42-、Cl-、OH- | B. | H+、I-、SO42-、NO3- | ||
| C. | Na+、OH-、SO42-、H2PO4- | D. | Ba2+、Na+、S2-、SO42- |
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:选择题
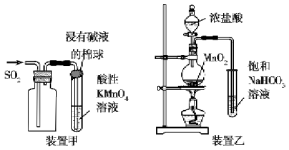
| A. | 装置甲收集SO2并验证其漂白性 | |
| B. | 装置乙验证氯气与水反应有盐酸生成 | |
| C. | 为河定新制氯水的pH,用玻璃棒蘸取液体滴在pH试纸上,与标准比色卡对照 | |
| D. | 证明Fe3-的氧化性大于Ⅰ2将KI溶液和FeCl3溶液在试管中混合后,加入CCl4,振荡、静置,下层溶液显紫红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 合金是由两种金属或两种非金属熔合而成的物质 | |
| B. | 合金的硬度较大,多数的合金的熔点比各成分的金属的低 | |
| C. | 根据所添加的元素的种类、含量来调节合金的性能 | |
| D. | 不锈钢在大气中比较稳定,不容易生锈,具有很强的抗腐蚀能力 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向待检液中加入BaCl2溶液有白色沉淀产生,再加盐酸,沉淀不消失,则原溶液中一定含有SO42- | |
| B. | 向待检液中加入NaOH溶液并加热,有能使湿润的红色石蕊试纸变蓝的气体生成,则原溶液中一定含有NH4+ | |
| C. | 向待检液中加入盐酸有能使澄清石灰水变浑浊的气体生成,则原溶液中一定含有大量的CO32- | |
| D. | 向待检液中加入几滴氯水,再加入KSCN溶液,溶液立即变红,则原溶液中一定含有Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制成合金保护船体 | B. | 锌块的反应:Zn-2e→Zn2 | ||
| C. | 船体的反应:Fe-2e→Fe2+ | D. | 是外加电流的阴极保护法 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.l mol•L-1的NaAlO2溶液:K+、Na+、SO42-、HCO3- | |
| B. | 在pH=1的溶液中:NH4+、Fe3+、SO42-、Cl- | |
| C. | 含有大量ClO-溶液中:K+、OH-、I-、SO32- | |
| D. | c(Cu2+)=0.1 mol•L-1的溶液中:Na+、Cl-、AlO2-、HS- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体颜色不再变化 | B. | 容器内压强不再变化 | ||
| C. | HI的体积分数不再变化 | D. | 2v正(H2)=v逆(HI) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、Al3+、NO3-、Cl- | B. | Na+、NO3-、K+、CH3COO- | ||
| C. | Na+、MnO4-、SO42-、K+ | D. | HCO3-、Cl-、K+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 呈弱酸性,使石蕊试液显浅红色 | |
| B. | 分子中的13个原子有可能处于同一平面 | |
| C. | 可以和NaHCO3溶液反应产生气体 | |
| D. | 能与FeCl3溶液反应生成紫色沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com