
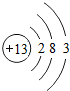 ,Al元素为13号元素,原子核外有13个电子,所以核外电子排布式为:1s22s22p63s23p1,自然界中的铝全部以铝土矿的形式存在;
,Al元素为13号元素,原子核外有13个电子,所以核外电子排布式为:1s22s22p63s23p1,自然界中的铝全部以铝土矿的形式存在;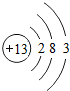 ,Al元素为13号元素,原子核外有13个电子,所以核外电子排布式为:1s22s22p63s23p1,自然界中的铝全部以铝土矿的形式存在,故答案为:三;ⅢA;1s22s22p63s23p1;铝土矿;
,Al元素为13号元素,原子核外有13个电子,所以核外电子排布式为:1s22s22p63s23p1,自然界中的铝全部以铝土矿的形式存在,故答案为:三;ⅢA;1s22s22p63s23p1;铝土矿;
| ||
| ||


科目:高中化学 来源: 题型:
| A、已知20℃时,KNO3的溶解度为31.6g.则20℃时KNO3饱和溶液的质量分数等于31.6% |
| B、1mol/L的食盐溶液中含有58.5gNaCl |
| C、所有物质的溶解度随着温度的升高而上升 |
| D、实验室需要230mL 0.1mol/L的H2SO4溶液,应选用250mL容量瓶配制 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,11.2 L Cl2通入含0.5molFeBr2的溶液中转移电子数为1.5NA |
| B、0.1 mol?L-1的AlCl3溶液与足量NaOH溶液反应所得产物中含AlO2-为0.1NA |
| C、足量Zn与浓硫酸共热可生成标准状况下的气体2.24 L,则参加反应的硫酸为0.4 NA |
| D、常温常压下,5.6g环丙烷和聚乙烯的混合物中含有的碳原子数为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素代号 | X | Y | Z | M | R |
| 原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
| 主要化合价 | +1 | +6-2 | +5-3 | -2 | +3 |
| A、离子半径大小:R3+<X+<M2- |
| B、Y与M组成的化合物是光化学烟雾的原因之一 |
| C、将YM2通入Ba(NO3)2溶液中有大量白色沉淀产生 |
| D、M氢化物的熔沸点高于Z氢化物的熔沸点 |
查看答案和解析>>
科目:高中化学 来源: 题型:
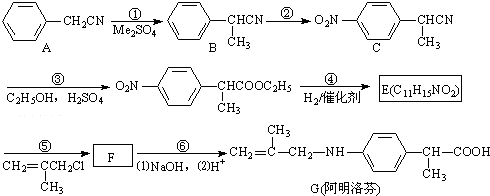
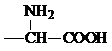 ②含有对位二取代苯环
②含有对位二取代苯环| 浓硫酸 |
| 170℃ |
| Br2 |

查看答案和解析>>
科目:高中化学 来源: 题型:
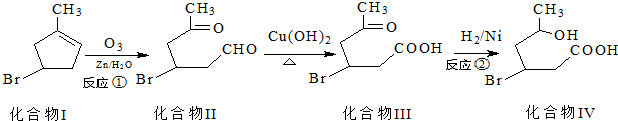
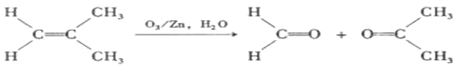
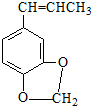 )发生类似反应①的反应,得到乙醛和化合物Y,Y的结构简式为
)发生类似反应①的反应,得到乙醛和化合物Y,Y的结构简式为查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验序号 | 待测液数据/mL | 标准液数据/mL | ||
| 滴定前 | 滴定后 | 取用前 | 取用后 | |
| 1 | 0.10 | 20.10 | 0.00 | 20.00 |
| 2 | 0.80 | 22.60 | 0.00 | 20.00 |
| 3 | 0.40 | 20.20 | 0.00 | 20.00 |
| 4 | 1.20 | 21.40 | 0.00 | 20.00 |
| A、0.1000 mol/L |
| B、0.0978 mol/L |
| C、0.9780 mol/L |
| D、0.1020 mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com