
����Ŀ���������ȣ�ClNO�������ںϳ�ϴ�Ӽ�����ý�������м��壬ijѧϰС����ʵ������Cl2��NO�Ʊ�ClNO���ⶨ�䴿�ȣ���������ʵ�飨�г�װ����ȥ����
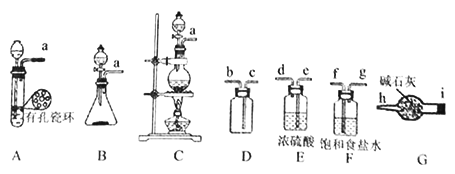
�������ϣ��������ȣ�ClNO�����۵�Ϊ-64.5�桢�е�Ϊ-5.5�棬��̬�ʻ�ɫ��Һ̬ʱ�ʺ��ɫ����ˮ��Ӧ����һ���⻯������ֵ��ij������������һ�ֳʺ���ɫ��
��ش��������⣺
��.Cl2���Ʊ������շ��������ķ���������ʵ������ȡ��������Ҫ����֮һ��
��1���÷�������ѡ����ͼ�е�________������ĸ��ţ�ΪCl2����װ�ã��÷�Ӧ�б������뱻��ԭ���ʵ����ʵ���֮��Ϊ_____________��
��2�����ռ�һƿ�����������ѡ����ͼ�е�װ�ã�������˳��Ϊ��a��____��i��h��������������Сд��ĸ��ţ���
���������ȣ�ClNO�����Ʊ���ʵ���ҿ�����ͼװ���Ʊ��������ȣ�ClNO����
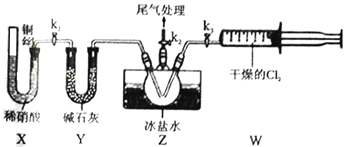
��3��ʵ����Ҳ����Bװ���Ʊ�NO����֮���X װ�õ��ŵ�Ϊ__________________________��
��4����װ��ʵ��װ�ú�Ӧ��____________��Ȼ������װ��ҩƷ����k2���ٴ�__________���k1����k3������ͨ��һ��ʱ�����壬��Ŀ����Ϊ���ž�������ƿ�еĿ�������ֹNO��ClNO ���ʡ�������,����������Z�з�Ӧ������Ϊ________________________________��
III���������ȣ�ClNO�����ȵIJⶨ���������������ȣ�ClNO����Ʒ13.10g����ˮ�����Ƴ�250mL��Һ��ȡ��25.00mL����K2CrO4��ҺΪָʾ������0.8mol��L-1AgNO3����Һ�ζ����յ㣬���ı���Һ�����Ϊ 22.50mL������֪��AgCrO4Ϊש��ɫ���壩
��5���������ȣ�ClNO����ˮ��Ӧ�Ļ�ѧ����ʽΪ_________________________��
��6���������ȣ�ClNO������������Ϊ______________________��
���𰸡� C 2:1 f��g��e��d��c��b �ų�װ���ڿ����ĸ��ţ������濪���ã������ͣ ���װ�õ������� k3 ���ֺ��ɫҺ�� 2ClNO+H2O=2H++2Cl-+NO��+NO2�� 90.0%
����������.(1)ʵ�����Ʊ������Ǽ��ȶ������̺�Ũ����Ļ���Ӧ��ѡ����ͼ�е�CΪCl2����װ�ã���Ӧ�ķ���ʽΪMnO2+4HCl![]() MnCl2+Cl2��+2H2O����Ӧ�ж������������������Ȼ����ǻ�ԭ�������뷴Ӧ���Ȼ���ֻ��һ�뱻���������������Ȼ����뱻��ԭ�Ķ������̵����ʵ���֮��Ϊ2:1���ʴ�Ϊ��C��2:1��
MnCl2+Cl2��+2H2O����Ӧ�ж������������������Ȼ����ǻ�ԭ�������뷴Ӧ���Ȼ���ֻ��һ�뱻���������������Ȼ����뱻��ԭ�Ķ������̵����ʵ���֮��Ϊ2:1���ʴ�Ϊ��C��2:1��
(2)�Ƶõ����������������Ȼ����ˮ��������Ҫ�ñ���ʳ��ˮ��ȥ�Ȼ��⣬����Ũ���������ռ�һƿ�����������ѡ����ͼ�е�װ�ã�������˳��Ϊ��a��f��g��e��d��c��b ��i��h���ʴ�Ϊ��f��g��e��d��c��b��
����(3)ʵ����Ҳ����Bװ���Ʊ�NO����֮���X װ�������ų�����װ���ڿ����ĸ��ţ������濪���ã������ͣ���ʴ�Ϊ�������ų�װ���ڿ����ĸ��ţ������濪���ã������ͣ��
(4)�漰����ķ�Ӧ����װ��ʵ��װ�ú�Ӧ�ȼ��װ�õ������ԣ�Ȼ������װ��ҩƷ����k2���ٴ�k3��ͨ��һ��ʱ�����壬��Ŀ����Ϊ���ž�������ƿ�еĿ�������ֹNO��ClNO ���ʡ�������������������Z�з�����Ӧ����ClNO����ȴ���ɺ��ɫҺ�壬�ʴ�Ϊ�����װ�õ������ԣ�k3�����ֺ��ɫҺ�壻
III��(5)��������(ClNO)��ˮ��Ӧ����һ���⻯������ֵ��ij������������һ�ֳʺ���ɫ��Ϊ�����������⻯��Ϊ�Ȼ��⣬���ݻ��ϼ۵ı仯����һ�ֵ���������Ϊһ������������������ˮ��Ӧ�Ļ�ѧ����ʽΪ2ClNO+H2O=2H++2Cl-+NO��+NO2�����ʴ�Ϊ��2ClNO+H2O=2H++2Cl-+NO��+NO2����
(6)�ζ��Ƿ����Ȼ����������������Ȼ�����ɫ�����ķ�Ӧ��������ש��ɫ���壬�Ұ����û�����Ա仯����ʾ�ﵽ�˵ζ��յ㣬n(Cl-)= n(Ag+)=0.0225L��0.8mol��L-1=0.018mol������������(ClNO)����������Ϊ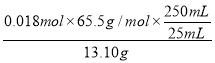 ��100%=90.0%���ʴ�Ϊ��90.0%��
��100%=90.0%���ʴ�Ϊ��90.0%��


 ��ѧ����ͬ����ϰϵ�д�
��ѧ����ͬ����ϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijԪ�ص�ԭ�Ӻ����������ܲ㣬�������4�����ӣ���ԭ�Ӻ��ڵ�������Ϊ
A. 14 B. 15 C. 16 D. 17
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E ���ֶ�����Ԫ�أ�A��B��C��D��E �ֱ����Ԫ�ط����������ǵ�ԭ�������������� A ��Ԫ�����ڱ���ԭ�Ӱ뾶��С��Ԫ����B Ԫ������������Ӧ��ˮ���������⻯�ﷴӦ����һ���� X��D �� A ͬ���������� E ͬ������E Ԫ��ԭ�ӵ�������������������������� 3/4 ����C �� E ͬ ���塣��ش��������⣺
��1��X �Ļ�ѧʽ_____��
��2�����и����У���˵��Ԫ�� C �� E �ǽ�����ǿ����ʵ��_____(�����).
�� �⻯��H2E�����Ա�H2Cǿ
�� �⻯��H2C�����ȶ��Ա�H2Eǿ
�� �⻯��H2E��ˮ��Һ�����ڿ����л�����
�� C �� E ��ɻ����C �Ը���
��3������ BC ��BC2��ɵĻ������ͨ����ͼ��ʾװ������������֤Ũ����������Ա�ϡ�����������ǿ��

��֪��i��Ũ�����ܽ����� BC ������BC2����ϡ��������� BC��
��ii��NaOH ��Һ��BC2��Ӧ�Ļ�ѧ����ʽΪ��2NaOH+2BC2�TNaBC2+NaBC+H2O��NaOH��Һ�� BC ���岻��Ӧ�� װ�â�������ʢ�ŵ�ҩƷ������_______��______________.
��4��ͨ��������֮ǰ��Ӧ��ͨ��һ��ʱ��ij����һ�����������Ʋ���ͨ��ĸ����������__________(�� һ������Ļ�ѧʽ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ȿ���ͨ�������뵥�ʻ��ϣ�Ҳ����ͨ����Һ�еĸ��ֽⷴӦ���ƵõĻ������ǣ� ��
A.Na2O
B.Na2O2
C.FeCl2
D.FeS
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������4�����ʣ���Na2O2����SiO2����SO2����NaHCO3���塣���У�
��1����ˮ��Ӧ��������ʹ������ľ����ȼ�Ĺ�����________������ţ���
��2����ʹƷ����Һ��ɫ�Ҽ���ʱ�ָ�ԭ����_________������ţ���
��3��������������1������������ˮ����������һ���������뽹̿������Ӧ�����Ƶõ���оƬ�Լ�̫���ܵ�صIJ������÷�Ӧ�Ļ�ѧ����ʽΪ��_______________________________��
��4��������������1�����ʿ���������ȥ�����θ�ᣬ�����dz��������ɼ�����Ҫ����Ϊ���ڼ��������²��������壬ʹʳƷ�����ɡ�д�������ȷֽ�Ļ�ѧ����ʽ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������о���һ�ֻ�������ȫ�Ĵ��ⷽ������ԭ���ɱ�ʾΪNaHCO3��H2 HCOONa��H2O�������й�˵������ȷ����(����)
HCOONa��H2O�������й�˵������ȷ����(����)
A. ���⡢������̾��������仯
B. ��������У�NaHCO3����ԭ
C. NaHCO3��HCOONa���������Ӽ����ۼ�
D. ��������У�ÿ����0.1 mol H2O�ų�2.24 L��H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���绯ѧ���������������ڼ�����NH3�ĺ������乤��ԭ��ʾ��ͼ���¡�����˵������ȷ���ǣ� ��

A. O2�ڵ缫b�Ϸ�����ԭ��Ӧ
B. ��Һ��OH����缫a�ƶ�
C. ��Ӧ���ĵ�NH3��O2�����ʵ���֮��Ϊ4��5
D. �����ĵ缫��ӦʽΪ2NH3��6e����6OH��===N2��6H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����û�ѧ��Ӧ�������������ڲ��Ļ�ѧ��ת��Ϊ���ܣ���ѧ����Ƴ���ԭ��أ��Ӷ�Ϊ���������������ṩ������
(1)��ͬѧ��Ϊ�����е�������ԭ��Ӧ��������Ƴ�ԭ��أ����Ƿ�ͬ�⣿________(����������������)��
(2)��ͬѧ����������ԭ��Ӧ��2Ag++Cu===Cu2++2Ag��Ƶ�ԭ�����ͼ��ʾ��

�ٸ���������_______�������ĵ缫��ӦΪ____________________________��
�����·�еĵ����Ǵ�________�缫����________�缫��(д���缫���ϵ�����)
�۵���Ӧ���е�һ��ʱ���ȡ���缫���ϣ����ijһ�缫������5.4 g�����ԭ��ط�Ӧ��ת�Ƶĵ�����Ŀ��________��
��.ˮ������֮Դ��Ҳ�ǻ�ѧ��Ӧ�е����ǡ���ش��������⣺
(1)��֪��2 mol H2��ȫȼ������Һ̬ˮʱ�ų�572 kJ��������
��������������ܺ�________(����>����<������=��)��Ӧ��������ܺ͡�
����2 mol������ȫȼ������ˮ��������ų�������________(����>����<������=��)572 kJ��
��ÿ������ȼ������Һ̬ˮʱ�ų�������Ϊ________��
(2)��Ȼ��(��Ҫ�ɷ�CH4)��������Ӧ���ɶ�����̼��ˮ���÷�ӦΪ���ȵ�������ԭ��Ӧ���ɽ�����Ƴ�ȼ�ϵ�أ�������ͼ��ʾ��a��b�����缫���ɶ��̼����ɡ�

a�缫�ĵ缫��Ӧʽ��_______________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)�ѱ�״����VL���壨Ħ������ΪMg��mol-1������1Lˮ�У������Ƿ�Ӧ����������Һ�ܶ�Ϊ��g/cm3�������Һ�����ʵ���Ũ��Ϊ_________________mol/L��
(2)��100mL0.3mol/LNa2SO4��Һ��400mL0.2mol/LNaCl��Һ��Ϻ���Һ��Na+�����ʵ���Ũ��Ϊ_____________________
(3)һ��������Al���������ᷴӦ����ת����2 mol����ʱ�����뷴Ӧ������������________g��
(4)�������ʣ���Fe ��NaCl ��Na2O ��CO ��CO2 ������ ��NH3 ��NaCl��Һ ������ �� H2SO4 Ba(OH)2
���ڵ���ʵ���_______ �� ���ڷǵ���ʵ��� ________���ܵ������_____________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com