
A、 电解精炼铝 |
B、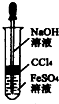 制备Fe(OH)2 |
C、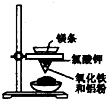 制得金属铁 |
D、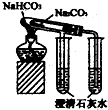 验证NaHC03和Na2C03的热稳定性 |


科目:高中化学 来源: 题型:
| A、CH4和C3H4,体积比为1:1 |
| B、C2H2和C2H6,体积比为3:1 |
| C、C2H4和C2H6,体积比为2:1 |
| D、C2H2 和C2H4,体积比为2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
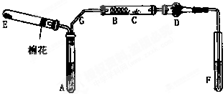 如图是某化学兴趣小组设计的乙醇催化氧化的实验装置(图中加热仪器、铁架台、试管夹均未画出).图中A处为无水乙醇(沸点78℃),B处为绕成螺旋状的细铜丝或银丝,C处为无水CuSO4粉末,D处为碱石灰,F处为新制的碱性Cu(OH)2悬浊液.
如图是某化学兴趣小组设计的乙醇催化氧化的实验装置(图中加热仪器、铁架台、试管夹均未画出).图中A处为无水乙醇(沸点78℃),B处为绕成螺旋状的细铜丝或银丝,C处为无水CuSO4粉末,D处为碱石灰,F处为新制的碱性Cu(OH)2悬浊液.查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 实验现象 | 结 论 |
| A | 将少量Fe(NO3)2试样加水溶解,滴加稀H2SO4酸化,再滴加KSCN溶液 | 溶液变成红色 | Fe(NO3)2试样已变质 |
| B | 将少量某无色气体通入澄清石灰水中 | 出现白色沉淀 | 该气体一定是CO2 |
| C | 分别测定常温下0.1mol?L-1Na2SiO3溶液和Na2CO3溶液的pH | pH:Na2SiO3>Na2CO3 | 非金属性:Si>C |
| D | 向浓度均为0.1mol?L-1NaCl和NaI混合溶液中,滴加少量AgNO3溶液 | 出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
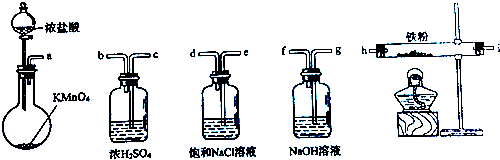
| A、a-b-c-d-e-e-f-g-h |
| B、a-e-d-c-b-h-i-g |
| C、a-d-e-c-b-h-i-g |
| D、a-c-b-d-e-h-i-f |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等于1:1 |
| B、小于1:1 |
| C、大于1:1 |
| D、小于或等于1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、3:5 | B、5:3 |
| C、5:8 | D、5:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 溶液 | 微粒 | 评价 |
| A | 8% H2O2水溶液 | Fe3+、Mg2+、SO42-、Na+ | 可以大量共存 |
| B | 室温下pH=12的水溶液 | NO3-、Na+、SO32-、K+ | NO3-能将SO32-氧化而不能大量共存 |
| C | 1 mol/L的NH4Cl溶液 | Ba2+、OH-、NH3?H2O、Na+ | NH4Cl溶液显酸性,NH3?H2O不能在其中大量共存 |
| D | NaHSO4水溶液 | I-、K+、CH3COO-、Br- | CH3COO-能与NaHSO4溶液反应,不能在其中大量共存 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com